��Ŀ����
����Ŀ��ʵ����ͨ����MnO2��Ũ���Ṳ����ȡCl2����Ӧ�Ļ�ѧ����ʽΪ
MnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O
MnCl2+Cl2��+2H2O
��1���÷�Ӧ���������� ����ԭ������ ����ԭ���� ������������ ��(�ѧʽ)
��2����˫���ŷ���ʾ�÷�Ӧ����ת�Ƶķ������Ŀ��MnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O
MnCl2+Cl2��+2H2O
(3)д��������ѧ����ʽ��Ӧ�����ӷ���ʽ ��
��4��������87.0gMnO2��ȫ�μӷ�Ӧ��������Ҫ����HCl�����ʵ����� mol�����ɵ������ڱ�״���µ������ L��
���𰸡�
��1��MnO2��MnCl2��HCl��Cl2��
��2��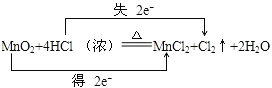
��3��MnO2+4H++2Cl-![]() Mn2++Cl2��+2H2O��4��4��22.4
Mn2++Cl2��+2H2O��4��4��22.4
��������
�����������1����ӦMnO2+4HCl�TMnCl2+Cl2+2H2O�У�MnԪ�ػ��ϼ۽��ͣ�����ԭ��MnO2Ϊ����������ԭ����ΪMnCl2��ClԪ�ػ��ϼ����ߣ���������Cl2Ϊ���������ԭ��ΪHCl���ʴ�Ϊ��MnO2��MnCl2��HCl��Cl2��
��2���������ͻ�ԭ����ʧ������Ŀ��ȣ���Ԫ�ػ��ϼ۵ı仯��֪ת�Ƶĵ�����ĿΪ2������˫���ŷ�����ʾ������ԭ��Ӧ�е���ת�����Ϊ�� ���ʴ�Ϊ��
���ʴ�Ϊ��  ��
��
(3)��Ӧ�����ӷ���ʽΪMnO2+4H++2Cl-![]() Mn2+ +Cl2��+2H2O���ʴ�Ϊ��MnO2+4H++2Cl-
Mn2+ +Cl2��+2H2O���ʴ�Ϊ��MnO2+4H++2Cl-![]() Mn2+ +Cl2��+2H2O��
Mn2+ +Cl2��+2H2O��
��4��87.0gMnO2�����ʵ���Ϊ![]() =1mol����ȫ��Ӧ��������Ҫ����HCl�����ʵ���Ϊ4mol������1mol�������ڱ�״���µ����Ϊ22.4L���ʴ�Ϊ��4��22.4��
=1mol����ȫ��Ӧ��������Ҫ����HCl�����ʵ���Ϊ4mol������1mol�������ڱ�״���µ����Ϊ22.4L���ʴ�Ϊ��4��22.4��

 ��У����ϵ�д�
��У����ϵ�д�