题目内容
4.下列各组中,每种电解质溶液电解时只生成氢气和氧气的是( )| A. | NaOH、H2SO4 | B. | NaOH、CuSO4 | C. | HCl、CuCl2 | D. | NaCl、AgNO3 |
分析 电解时只生成H2和O2,相当于电解水,应为强碱、含氧酸以及活泼金属的含氧酸盐的电解.
解答 解:A.电解NaOH、H2SO4,两极上分别生成H2和O2,故A正确;
B.电解CuSO4阴极生成Cu,故B错误;
C.电解HCl溶液生成H2和Cl2,电解CuCl2生成Cu和Cl2,故C错误;
D.电解NaCl,在阳极上生成Cl2,电解AgNO3,在阴极上得到银,故D错误.,
故选A.
点评 本题考查电解知识,侧重于电解规律的考查,注意把握离子放电顺序即可解答该题,题目难度不大.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
14.四氯化碳是生产金属钛及其化合物的重要中间体,实验窒利用反应:TiO2(s)+2CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),制取TiCl4,实验装置如图所示: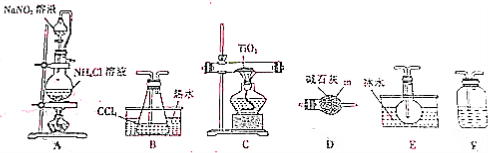
有关物质的性质如下表:
回答下列问题:
(1)仪器m的名称为球形干燥管.
(2)装置A中有氮气生成,该反应的化学方程式为NaNO2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+NaCl+2H2O
(3)实验装置依次连接的顺序为A→F→B→C→E→D.装置F中盛有的物质是浓硫酸(4)装置D的作用是防止外界的水汽进入TiCl4收集装置里.
(5)欲分离装置E中的液态混合物,所采用操作的名称是蒸馏.
(6)反应结束前进行如下操作:①停止通氮气②熄灭酒精灯③冷却至室温,正确的操作顺序是②③①(填序号)
(7)利用反应:TiO2(s)+2C(s)+2Cl2(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+2CO(g),也可以制取TiCl4,除了在上述实验装置中将装置A改为氯气的发生装置,撤去装置B之外,请简述对其他装置的改变:石英管内改为盛TiO2和C;增加CO的吸收装置;.

有关物质的性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 其它 |
| CCl4 | -23 | 76 | 与 TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾,加热时能被氧气氧化 |
(1)仪器m的名称为球形干燥管.
(2)装置A中有氮气生成,该反应的化学方程式为NaNO2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+NaCl+2H2O
(3)实验装置依次连接的顺序为A→F→B→C→E→D.装置F中盛有的物质是浓硫酸(4)装置D的作用是防止外界的水汽进入TiCl4收集装置里.
(5)欲分离装置E中的液态混合物,所采用操作的名称是蒸馏.
(6)反应结束前进行如下操作:①停止通氮气②熄灭酒精灯③冷却至室温,正确的操作顺序是②③①(填序号)
(7)利用反应:TiO2(s)+2C(s)+2Cl2(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+2CO(g),也可以制取TiCl4,除了在上述实验装置中将装置A改为氯气的发生装置,撤去装置B之外,请简述对其他装置的改变:石英管内改为盛TiO2和C;增加CO的吸收装置;.
15.下列各组物质不 属于同系物的是( )
| A. | 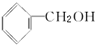 和 和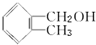 | B. | HOCH2-CH2OH和 | C. | CH3CH2OH和 | D. | HOCH2CH2OH和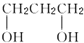 |
19.为提纯表中的物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
| 编号 | 被提纯物质 | 除杂试剂 | 分离方法 |
| ① | 苯甲酸(不溶于水的杂质) | 水 | 过滤、重结晶 |
| ② | 乙酸乙酯(醋酸) | 氢氧化钠溶液 | 分液 |
| ③ | 乙醇(4%的水) | 生石灰 | 蒸馏 |
| ④ | 二氧化碳(氯化氢) | 饱和碳酸钠溶液 | 洗气 |
| A. | ①② | B. | ①③ | C. | ②③ | D. | ③④ |
16.下列变化属于吸热反应的是( )
| A. | 碘的升华 | B. | Ba(OH)2•8H2O与NH4Cl混合搅拌 | ||
| C. | 生石灰与水反应 | D. | 浓硫酸稀释 |
 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)△H<0
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)△H<0 FeCl3溶液可用作印刷电路铜板的腐蚀剂,该腐蚀过程的离子方程式为2Fe3++Cu=2Fe2++Cu2+.若将该反应设计成原电池,请在如图方框中画出原电池的装置简图,标出正、负极及两极材料和电解质溶液.
FeCl3溶液可用作印刷电路铜板的腐蚀剂,该腐蚀过程的离子方程式为2Fe3++Cu=2Fe2++Cu2+.若将该反应设计成原电池,请在如图方框中画出原电池的装置简图,标出正、负极及两极材料和电解质溶液. .
.