题目内容
相同体积的pH=1的强酸溶液和弱酸溶液分别与足量的锌完全反应,下列说法正确的是( )
| A、强酸溶液产生的H2多 |
| B、弱酸溶液产生的H2多 |
| C、两者产生的H2一样多 |
| D、无法比较 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:pH=1的强酸和弱酸,弱酸中存在电离平衡,则强酸浓度小于弱酸,等体积等pH的强弱酸,弱酸的物质的量大于强酸,与足量锌反应生成氢气的量与酸的物质的量成正比.
解答:
解:pH=1的强酸和弱酸,弱酸中存在电离平衡,所以c(强酸)<c(弱酸),反应过程中,弱酸能继续电离出氢离子,所以等体积等pH的强弱酸,弱酸中氢离子的物质的量大于强酸中氢离子的物质的量,与足量锌反应生成氢气的量与氢离子的物质的量成正比,所以弱酸溶液产生的氢气多,
故选B.
故选B.
点评:本题考查了弱电解质的电离,明确生成氢气的量与氢离子的关系是解本题关键,结合弱电解质电离特点来分析解答,难度不大.

练习册系列答案
相关题目
Li-Al/FeS电池是一种正在开发的车载电池,它的电池总反应方程式为:2Li+FeS=Li2S+Fe,有关该电池的下列说法中,不正确的是( )
| A、该电池中正极的电极反应式为:2Li++FeS+2e-=Li2S+Fe |
| B、Li-Al合金在电池中作为负极材料 |
| C、负极的电极反应式为Al-3e-=Al3+ |
| D、充电时,阳极发生的电极反应式为:Li2S+Fe-2e-=2Li++FeS |
下列离子方程式正确的是( )
A、石灰乳与Na2CO3溶液混合:Ca 2++C
| ||||
B、向沸水中滴加FeCl3溶液并加热制备Fe(OH)3胶体:Fe3++3H2O
| ||||
C、向CH2BrCOOH中加足量的氢氧化钠溶液并加热:CH 2BrCOOH+2OH-
| ||||
| D、FeO与稀硝酸反应:FeO+6H++NO3-=Fe3++NO↑+3H2O |
下列溶液均处于25℃,有关叙述正确的是( )
| A、将醋酸溶液加水稀释1000倍,pH增大3 |
| B、在NaHCO3溶液中,c(Na+)=c(HCO3-)+c(H2CO3) |
| C、pH=8的Ba(OH)2溶液和pH=8的氨水中,由水电离的c(OH-)均为1×10-8mo1?L-1 |
| D、pH=13的NaOH溶液与pH=1的盐酸混合后,一定有c(H+)=c(OH-) |

 ,则E的结构简式为
,则E的结构简式为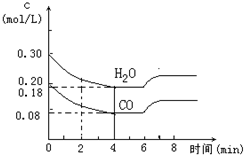
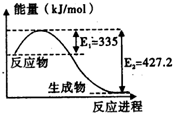 (1)已知:C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
(1)已知:C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol 完成下列各题:
完成下列各题: