题目内容
10.所含分子数相同的一组物质是( )| A. | 10g H2和10g N2 | B. | 1mol H2O和1g H2O | ||
| C. | 3.2g O2和2.24L的空气 | D. | 22gCO2和3.01×1023个O2 |
分析 所含分子数相同,说明二者的物质的量相等,根据n=$\frac{N}{{N}_{A}}$=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$进行计算.
解答 解:所含分子数相同,说明二者的物质的量相等,
A.根据n=$\frac{m}{M}$知,相同质量时,不同气体的物质的量与其摩尔质量成反比,氢气和氮气的摩尔质量不等,所以其物质的量不等,则分子数不等,故A错误;
B.1gH2O的n(H2O)=$\frac{1g}{18g/mol}$=$\frac{1}{18}$mol,二者的物质的量不等,则分子数不等,故B错误;
C.空气的状态不知,所以无法由体积由物质的量,故C错误;
D.22gCO2的n(CO2)=$\frac{22g}{44g/mol}$=0.5mol,n(O2)=$\frac{3.01×1{0}^{23}}{6.02×1{0}^{23}/mol}$=0.5mol,二者的物质的量相等,所以其分子数相等,故D正确;
故选D.
点评 本题考查了物质的量的有关计算,熟悉n、m、M、V、N之间的关系即可解答,注意C选项,1mol任何气体在标况下体积为22.4L,“任何气体”指纯净物或混合物,为易错点.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
18.在两个密闭容器中,分别充有质量相等的甲、乙两种气体,它们的温度和密度均相同.试根据甲、乙的摩尔质量(M)的关系,判断下列说法中正确的是( )
| A. | 若M(甲)>M(乙),则分子数:甲>乙 | B. | 若M(甲)<M(乙),则气体摩尔体积:甲>乙 | ||
| C. | 若M(甲)<M(乙),则气体的压强:甲>乙 | D. | 若M(甲)>M(乙),则气体体积:甲<乙 |
5.除去下列括号内杂质的试剂或方法错误的是( )
| A. | MgO固体(SiO2),加过量NaOH溶液充分反应,过滤、洗涤、干燥 | |
| B. | CO2(SO2),酸性KMnO4溶液、浓硫酸,洗气 | |
| C. | KNO3晶体(NaCl),蒸馏水溶解、蒸发、结晶、过滤、洗涤、干燥 | |
| D. | FeCl3溶液(CuCl2),过量铁粉,过滤 |
15.下列反应属于氧化还原反应的是( )
| A. | HCl+NaOH═NaCl+H2O | B. | SO3+H2O═H2SO4 | ||
| C. | 2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ |
2.对于下列事实的解释错误的是( )
| A. | 浓硫酸使胆矾晶体的蓝色褪去,说明浓硫酸具有吸水性 | |
| B. | 豆科植物根部的根瘤菌可以将空气中的氮由游离态转为化合态是氮的固定 | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 | |
| D. | 氨水可使酚酞试剂变为红色,说明氨水显碱性 |
4.下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A. | 氢氧化钠与盐酸;氢氧化铜与盐酸 | B. | BaCl2与Na2SO4;Ba(OH)2与H2SO4 | ||
| C. | Na2CO3与硝酸;CaCO3与硝酸 | D. | 石灰石与硝酸反应;石灰石与盐酸 |
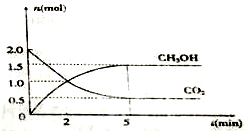 “低碳循环”引起了全世界的高度重视,减排CO2的一种方法是:
“低碳循环”引起了全世界的高度重视,减排CO2的一种方法是: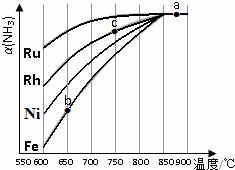 氨气在生产、生活和科研中应用十分广泛
氨气在生产、生活和科研中应用十分广泛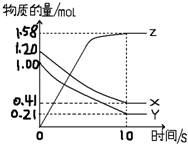 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示: