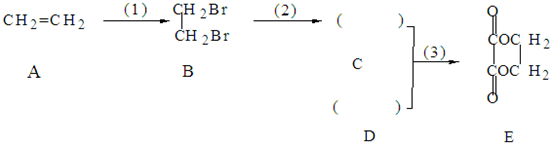题目内容
下列有关氯水的叙述,正确的是( )
| A、新制氯水中只含有氯气和次氯酸分子 |
| B、新制氯水可使紫色石蕊试液先变红后褪色 |
| C、氯水光照时有气泡逸出,该气体的主要成分是氯气 |
| D、氯水放置数天后,其导电能力减弱 |
考点:氯气的化学性质
专题:卤族元素
分析:由氯气溶于水,部分氯气与水反应发生反应:Cl2+H2O?HCl+HClO,HClO?H++ClO-,HCl=H++Cl-,所以氯水中存在Cl2、H2O、HClO、H+、Cl-、ClO-、OH-,利用离子、分子的性质来分析.
解答:
解:A.新制氯水中只含有氯气、次氯酸、水三种分子,H+、Cl-、ClO-、OH-四种离子,故A错误;
B.新制氯水中含盐酸,使石蕊变红,含HClO使石蕊褪色,可使紫色石蕊试液先变红后褪色,故B正确;
C.氯水光照时有气泡逸出,发生2HClO
2HCl+O2↑,故C错误;
D.氯水放置数天后,发生2HClO
2HCl+O2↑,为盐酸溶液,离子浓度增大,其导电能力增大,故D错误;
故选B.
B.新制氯水中含盐酸,使石蕊变红,含HClO使石蕊褪色,可使紫色石蕊试液先变红后褪色,故B正确;
C.氯水光照时有气泡逸出,发生2HClO
| ||
D.氯水放置数天后,发生2HClO
| ||
故选B.
点评:本题考查氯气的化学性质,为高频考点,把握氯气的性质及氯水的成分为解答的关键,注意HClO的不稳定和漂白性,题目难度不大.

练习册系列答案
相关题目
四种短周期元素在周期表中的位置如图,其中Y元素被称为“国防金属”.下列说法不正确是( )
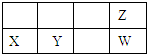

A、X离子结构示意图: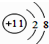 |
| B、原子半径Y比Z大 |
| C、元素的气态氢化物的稳定性Z强于W |
| D、X和Y两元素的最高价氧化物的对应水化物能相互反应 |
下列实验操作中,所用仪器合理的是( )
| A、用托盘天平称取25.20gNaCl |
| B、用四氯化碳萃取碘的饱和水溶液中的碘分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出. |
| C、在蒸发皿中放入NaCl溶液,加热、蒸发制取NaCl晶体 |
| D、用100mL容量瓶配制50mL0.1mol/L的盐酸 |
醋酸在水溶液中存在下列电离平衡:CH3COOH?CH3COO-+H+下列说法不正确的是( )
| A、加入醋酸钠,平衡向左移动 |
| B、加入碳酸钠,平衡向右移动 |
| C、加水稀释,C(H+)减小 |
| D、加水稀释,溶液中仅有的三种离子浓度都减小 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、24g镁单质变为镁离子时,失去的电子数为2NA |
| B、18g水中所含原子总数为NA |
| C、22.4L甲烷中所含原子总数为5NA |
| D、H2SO4的摩尔质量为98g |
下列说法中正确的是( )
| A、在热化学方程式中无论反应物还是生成物必须标明聚集状态 |
| B、热化学方程式的化学计量数可表示分子的个数 |
| C、反应热指的是反应过程中放出的热量 |
| D、所有的化学反应都伴随光能变化 |
一小块钠置于空气中,有下列现象:①变成白色粉末,②变暗,③变成白色固体,④变成液体,上述现象出现的先后顺序是 ( )
| A、①②③④ | B、②③④① |
| C、②③①④ | D、③②④① |
下列反应中,同一种物质既做氧化剂又做还原剂的是( )
A、CaCO3
| ||||
B、2NaHCO3
| ||||
| C、Cl2+H2O═HCl+HClO | ||||
| D、H2+Cl2═2HCl |