题目内容
印刷电路板由高分子材料和铜箔组成,刻制印刷电路时,用FeCl3作为腐蚀液,写出反应的化学方
程式,并标出化合价的变化. .
程式,并标出化合价的变化.
考点:化学方程式的书写,铁盐和亚铁盐的相互转变
专题:元素及其化合物
分析:Cu具有还原性、FeCl3具有氧化性,二者发生氧化还原反应生成CuCl2、FeCl2,反应方程式为2FeCl3+Cu=CuCl2+2FeCl2 .
解答:
解:Cu具有还原性、FeCl3具有氧化性,二者发生氧化还原反应生成CuCl2、FeCl2,反应方程式为2FeCl3+Cu=CuCl2+2FeCl2 ,该反应中Cu元素化合价由0价变为+2价、Fe元素化合价由+3价变为+2价,其化合价变化为
+2
Cl3=2
Cl2+2
Cl2,故答案为:
+2
Cl3=2
Cl2+2
Cl2.
| 0 |
| Cu |
| +3 |
| Fe |
| +2 |
| Cu |
| +2 |
| Fe |
| 0 |
| Cu |
| +3 |
| Fe |
| +2 |
| Cu |
| +2 |
| Fe |
点评:本题以亚铁盐和铁盐为载体考查氧化还原反应方程式的书写,明确物质的性质是解本题关键,知道常见元素化合价,题目难度不大.

练习册系列答案
相关题目
下列物质属于芳香烃,但不是苯的同系物的是( )
①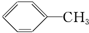 ②
②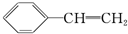 ③
③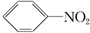 ④
④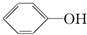 ⑤
⑤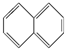 ⑥
⑥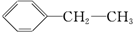
①
 ②
②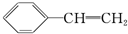 ③
③ ④
④ ⑤
⑤ ⑥
⑥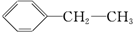
| A、③④ | B、②⑤ |
| C、①②⑤⑥ | D、②③④⑤⑥ |
下列离子方程式书写正确的是( )
| A、石灰乳与Na2CO3溶液混合:Ca2++CO32-═CaCO3↓ | ||||
B、NH4HSO3溶液与足量的NaOH溶液混合加热:NH4++HSO3-+2OH-
| ||||
| C、酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O═3I2+6OH- | ||||
| D、AgNO3溶液中加入过量的氨水:Ag++NH3?H2O═AgOH↓+NH4+ |
下列离子方程式书写正确的是( )
| A、在FeCl3溶液中加入铁粉:Fe3++Fe=2Fe2+ |
| B、锌与18.4mol?L的H2SO4溶液反应:Zn+2H+=Zn2++H2↑ |
| C、用NaOH溶液吸收氯气:C12+2OH-=Cl-+ClO-+H2O |
| D、稀H2SO4与Ba(OH)2溶液反应:Ba2++OH-+SO42-+H+=BaSO4↓+H2O |

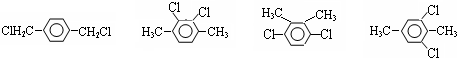 外,还有
外,还有