题目内容
一个体重50kg的健康人含Fe元素约2g.主要以Fe2+、Fe3+形式存在于人体内.Fe2+易被吸收,给贫血者补充铁时,应补充Fe2+的亚铁盐(如FeSO4).服用Vitc,可使食物中的Fe3+转化为Fe2+.
(1)人体中经常进行Fe2+
Fe3+的转化,在过程A中,Fe2+做 剂,过程B中Fe3+被 .
(2)Vitc使Fe3+转化为Fe2+Vitc在这一过程中做 ,具有 性.
(1)人体中经常进行Fe2+
| A |
| B |
(2)Vitc使Fe3+转化为Fe2+Vitc在这一过程中做
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)过程A中Fe元素的化合价升高,过程B中Fe元素的化合价降低;
(2)Vitc使Fe3+转化为Fe2+,Fe元素的化合价降低,则Vitc在这一过程中某元素的化合价升高.
(2)Vitc使Fe3+转化为Fe2+,Fe元素的化合价降低,则Vitc在这一过程中某元素的化合价升高.
解答:
解:(1)过程A中Fe元素的化合价升高,则Fe2+做还原剂;过程B中Fe元素的化合价降低,则Fe3+作氧化剂,被还原,故答案为:还原;还原;
(2)Vitc使Fe3+转化为Fe2+,Fe元素的化合价降低,则Vitc在这一过程中某元素的化合价升高,则作还原剂,具有还原性,故答案为:还原剂;还原.
(2)Vitc使Fe3+转化为Fe2+,Fe元素的化合价降低,则Vitc在这一过程中某元素的化合价升高,则作还原剂,具有还原性,故答案为:还原剂;还原.
点评:本题考查氧化还原反应,为高频考点,侧重于学生的分析能力和应用能力的考查,明确反应中元素的化合价变化是解答的关键,题目难度不大.

练习册系列答案
相关题目
NA为阿伏加德罗常数,下列叙述错误的是( )
| A、18g H2O中含的质子数为10NA |
| B、标准状况下,11.2L SO3中所含分子数目为0.5NA |
| C、46g NO2和N2O4混合气体中含有原子总数为3NA |
| D、132g硫酸铵中含有氮原子数目为2NA |
下列各组物质的关系中,其中属于同分异构体的是( )
| A、O2 和O3 |
| B、16O 和18O |
| C、正丁烷和异丁烷 |
| D、甲烷和乙烷 |
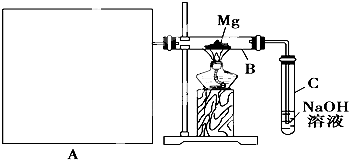 已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性.
已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性.