题目内容
(1)下列物质:①H2O ②铜 ③小苏打 ④稀硫酸 ⑤CH3COOH ⑥酒精 属于强电解质的是 ;属于弱电解质的是 ;属于非电解质的是 (用编号填写).
(2)在下列的空白处填写最适宜的除杂试剂或方法
①小苏打溶液中含少量苏打 ,
②苏打固体中含少量小苏打 ,
③Cl2气体中混有少量的HCl气体 .
(2)在下列的空白处填写最适宜的除杂试剂或方法
①小苏打溶液中含少量苏打
②苏打固体中含少量小苏打
③Cl2气体中混有少量的HCl气体
考点:电解质与非电解质,强电解质和弱电解质的概念,物质的分离、提纯和除杂
专题:
分析:(1)强电解质:溶于水的部分或者熔融状态时,可以完全变成阴阳离子的化合物,一般是强酸、强碱和大部分盐类;
弱电解质:只有部分电离的电解质,如弱酸、弱碱和水等;
非电解质:在水溶液里或熔融状态下都不能导电的化合物,包括非金属氧化物、部分氢化物和一些有机物,如乙醇、蔗糖;
单质和混合物既不是电解质也不是非电解质;
(2)①Na2CO3溶液可与二氧化碳反应生成NaHCO3;
②加热NaHCO3分解生成Na2CO3;
③HCl易溶于水,而氯气难溶于饱和食盐水,所以可用饱和NaCl溶液除去Cl2中的少量HCl.
弱电解质:只有部分电离的电解质,如弱酸、弱碱和水等;
非电解质:在水溶液里或熔融状态下都不能导电的化合物,包括非金属氧化物、部分氢化物和一些有机物,如乙醇、蔗糖;
单质和混合物既不是电解质也不是非电解质;
(2)①Na2CO3溶液可与二氧化碳反应生成NaHCO3;
②加热NaHCO3分解生成Na2CO3;
③HCl易溶于水,而氯气难溶于饱和食盐水,所以可用饱和NaCl溶液除去Cl2中的少量HCl.
解答:
解:(1)①H2O部分电离,是弱电解质;
②铜是单质,既不是电解质也不是非电解质;
③NaHCO3在水溶液中完全电离,是强电解质;
④稀硫酸属于混合物,既不是电解质也不是非电解质;
⑤CH3COOH在水溶液中部分电离,是弱电解质;
⑥酒精在熔融状态和水溶液中都不能导电,是非电解质;
故属于强电解质的是:③,属于弱电解质的是:①⑤,属于非电解质的是:⑥,
故答案为:③;①⑤;⑥;
(2)①Na2CO3溶液可与二氧化碳反应生成NaHCO3,因此可通入过量二氧化碳除杂,
故答案为:二氧化碳;
②加热NaHCO3分解生成二氧化碳、水、Na2CO3,因此可用加热的方法使“杂变纯”
故答案为:加热;
③HCl易溶于水,而氯气难溶于饱和食盐水,所以可用饱和NaCl溶液除去Cl2中的少量HCl,
故答案为:饱和食盐水.
②铜是单质,既不是电解质也不是非电解质;
③NaHCO3在水溶液中完全电离,是强电解质;
④稀硫酸属于混合物,既不是电解质也不是非电解质;
⑤CH3COOH在水溶液中部分电离,是弱电解质;
⑥酒精在熔融状态和水溶液中都不能导电,是非电解质;
故属于强电解质的是:③,属于弱电解质的是:①⑤,属于非电解质的是:⑥,
故答案为:③;①⑤;⑥;
(2)①Na2CO3溶液可与二氧化碳反应生成NaHCO3,因此可通入过量二氧化碳除杂,
故答案为:二氧化碳;
②加热NaHCO3分解生成二氧化碳、水、Na2CO3,因此可用加热的方法使“杂变纯”
故答案为:加热;
③HCl易溶于水,而氯气难溶于饱和食盐水,所以可用饱和NaCl溶液除去Cl2中的少量HCl,
故答案为:饱和食盐水.
点评:本题考查强弱电解质、非电解质概念的辨析,以及杂质的去除,难度中等,要注意除杂时,不能引入新的杂质.

练习册系列答案
相关题目
下列关于胶体的叙述不正确的是( )
| A、利用丁达尔现象可以区别溶液和胶体 |
| B、胶体都可以发生丁达尔现象 |
| C、胶体粒子的大小都在1nm-100nm之间 |
| D、加热氢氧化铁胶体没有明显现象 |
下列各组离子因为生成难溶物而不能大量共存的是( )
| A、Cl-、Fe3+、NO3-、OH- |
| B、HCO3-、Cl-、Na+、H+ |
| C、Ba2+、Cl-、NO3-、K+ |
| D、NH4+、K+、OH-、Cl- |
以下实验原理或操作中,正确的是( )
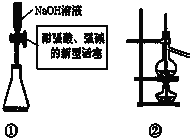

| A、装置①量取15.00 mLNaOH溶液 |
| B、装置②既可用于乙醇制乙烯的发生装置,又可用于分离沸点相差较大的互溶液体混合物 |
| C、室温下,含有CoCl2的干燥变色硅胶呈蓝色,在潮湿的空气中变粉红色,放在干燥的空气中又恢复为蓝色 |
| D、纸层析法分离铁离子和铜离子实验中,展开剂的成份为蒸馏水与丙酮 |
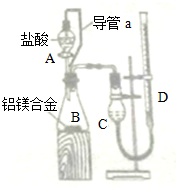

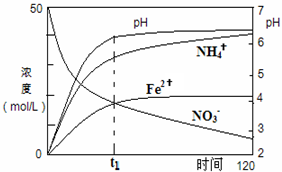 氮元素的化合物在工农业以及国防科技中用途广泛,但也会对环境造成污染,如地下水中硝酸盐造成的氮污染已成为一个世界性的环境问题.
氮元素的化合物在工农业以及国防科技中用途广泛,但也会对环境造成污染,如地下水中硝酸盐造成的氮污染已成为一个世界性的环境问题.