题目内容
下列方程式书写不正确的是( )
| A、碳酸的电离方程式:H2CO3?2H++CO32- |
| B、向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| C、明矾水解:Al3++3H2O?Al(OH)3+3H+ |
| D、铅酸蓄电池充电时的正(阳)极反应:PbSO4+2H2O-2e-=PbO2+4H++SO42- |
考点:离子方程式的书写
专题:
分析:A.碳酸为二元若弱酸,以第一步电离为主;
B.氢氧化钡和硫酸反应生成硫酸钡和水;
C.铝离子水解生成氢氧化铝和氢离子;
D.充电时,阳极发生氧化反应生成PbO2.
B.氢氧化钡和硫酸反应生成硫酸钡和水;
C.铝离子水解生成氢氧化铝和氢离子;
D.充电时,阳极发生氧化反应生成PbO2.
解答:
解:A.碳酸为二元若弱酸,以第一步电离为主,应为H2CO3?H++HCO3-,故A错误;
B.氢氧化钡和硫酸反应生成硫酸钡和水,离子方程式为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故B正确;
C.铝离子水解生成氢氧化铝和氢离子,离子方程式为Al3++3H2O?Al(OH)3+3H+,故C正确;
D.充电时,阳极发生氧化反应生成PbO2,电极方程式为PbSO4+2H2O-2e-=PbO2+4H++SO42-,故D正确.
故选A.
B.氢氧化钡和硫酸反应生成硫酸钡和水,离子方程式为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故B正确;
C.铝离子水解生成氢氧化铝和氢离子,离子方程式为Al3++3H2O?Al(OH)3+3H+,故C正确;
D.充电时,阳极发生氧化反应生成PbO2,电极方程式为PbSO4+2H2O-2e-=PbO2+4H++SO42-,故D正确.
故选A.
点评:本题考查离子反应方程式的书写,为高频考点,侧重于学生的分析能力的考查,明确发生的化学反应是解答本题的关键,并注意离子反应的书写方法来解答,难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
下列解释事实的化学用语不正确的是( )
| A、生活中用纯碱做洗涤剂的原理:CO32-+H2O?HCO3-+OH- |
| B、已知某温度和压强下,将0.5molN2和1.5mol H2置于密闭容器中充分反应生成NH3(g)放热19.3KJ,故有:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ?mol-1 |
| C、“NO2球”浸泡在冷水中,颜色变浅:2NO2(g)?N2O4(g)△H<0 |
| D、NaHSO3溶液呈酸性:HSO3-+H2O?SO32-+H3O+ |
在一定温度下,CO和CH4燃烧的热化学方程式分别为:2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
CH4(g)+O2(g)═
CO2(g)+H2O(l)△H=-445kJ/mol,1molCO和2mol CH4组成的混合气体,在相同条件下完全燃烧时,释放的热量为( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、2346 kJ |
| B、2670 kJ |
| C、1698kJ |
| D、2063 kJ |
用足量的碳粉还原1mol金属氧化物,经充分反应生成的CO和CO2在标准状况下共40.32L,该金属氧化物可能是( )
| A、CuO |
| B、Fe3O4 |
| C、Al2O3 |
| D、PbO2 |
下列关于能量转换的认识中,不正确的是( )
| A、电解水生成氢气和氧气时,电能转化为化学能 |
| B、绿色植物进行光合作用时,太阳能转化为化学能 |
| C、每个化学反应都伴随着能量的变化 |
| D、当反应物浓度等于生成物浓度时,可逆反应一定已达到化学平衡状态 |
下列反应属于氧化还原反应的是( )
| A、14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4 | ||||
B、MgCl2(熔融)
| ||||
| C、CaCO3+2HCl═CaCl2+CO2↑+H2O | ||||
| D、Na2O+H2O═2NaOH |
某反应过程能量变化如图所示,下列说法正确的是( )
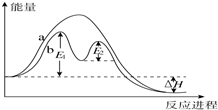

| A、反应过程a有催化剂参与 |
| B、该反应为放热反应,热效应不等于△H |
| C、使用催化剂,可改变该反应的活化能 |
| D、有催化剂条件下,反应的活化能等于E1-E2 |
下列粒子浓度关系不正确的是( )
| A、0.1mol/L的醋酸溶液中:c(CH3COOH)>c(H+)>c(CH3COO-) |
| B、0.1mol/L的明矾[KAl(SO4)2?12H2O]溶液中:c(SO42-)>c(K+)>c(Al3+)>c(H+)>c(OH-) |
| C、等浓度的Na2CO3与NaHCO3混合溶液中:c(Na+)+c(H+)=c(HCO3-)+2 c(CO32-)+c(OH-) |
| D、稀硫酸中滴入氨水至中性后所得的溶液中:c(NH4+)=c(SO42-)>c(H+)=c(OH-) |