题目内容
350体积(标况下)的氨气溶解在1体积的水里,求这种氨水的溶质质量分数和物质的量浓度(该氨水的密度为0.924g/mL)
考点:物质的量浓度的相关计算
专题:常规题型,计算题
分析:令NH3的体积为350L、水的体积为1L,根据n=
计算NH3的物质的量,根据m=nM计算HCl的质量,由m=ρV计算水的质量,NH3的质量分数
×100%;
再根据V=
计算溶液的体积,根据c=
计算所得溶液的物质的量浓度.
| V |
| Vm |
| m(NH3) |
| m(NH3)+m(H2O) |
再根据V=
| m |
| ρ |
| n |
| V |
解答:
解:设NH3的体积为350 L,水的体积为1 L,则:
n(NH3)=
=15.625 mol
溶液的质量=m(NH3)+m(H2O)=15.625 mol×17 g/mol+1 000 g≈1265.6 g
故溶液质量分数=
×100%=21%
溶液体积V=1265.6 g÷0.924 g/mL×10-3L/mL≈1.17 L
c(NH3)=15.625 mol÷1.17 L≈13.4 mol/L,
答:此溶液中HCl的质量分数为21%,物质的量浓度为13.4mol/L.
n(NH3)=
| 350L |
| 22.4l/mol |
溶液的质量=m(NH3)+m(H2O)=15.625 mol×17 g/mol+1 000 g≈1265.6 g
故溶液质量分数=
| 15.625mol×17g/mol |
| 1265.6g |
溶液体积V=1265.6 g÷0.924 g/mL×10-3L/mL≈1.17 L
c(NH3)=15.625 mol÷1.17 L≈13.4 mol/L,
答:此溶液中HCl的质量分数为21%,物质的量浓度为13.4mol/L.
点评:本题考查溶液浓度有关计算,涉及物质的量浓度、质量分数计算,难度不大,注意对公式的理解与灵活应用,注意掌握质量分数与物质的量浓度关系.

练习册系列答案
相关题目
下列物质中,碱性最强的是( )
| A、Mg(OH)2 |
| B、NaOH |
| C、KOH |
| D、LiOH |
用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作中不正确的是( )
| A、酸式滴定管用蒸馏水洗净后,必须用已知浓度的盐酸润洗 |
| B、锥形瓶用蒸馏水洗净后,用NaOH溶液润洗后再加入待测液 |
| C、滴定时,必须逐出滴定管下口的气泡 |
| D、读数时,视线与滴定管内液体的凹液面最低处保持水平 |
下列说法正确的是( )
| A、液态氯化氢、固态氯化钠不导电,所以HCl、NaCl不是电解质 |
| B、NH3、CO2水溶液均能导电,所以NH3、CO2均是电解质 |
| C、蔗糖、酒精在水溶液中或熔化时不导电,所以它们不是电解质 |
| D、铜、石墨均导电,所以它们是电解质 |
下面有关Na2CO3与NaHCO3的说法正确的是( )
| A、热稳定性:NaHCO3>Na2CO3 |
| B、相同浓度溶液的碱性:Na2CO3<NaHCO3 |
| C、都能与酸反应放出CO2,但剧烈程度:NaHCO3>Na2CO3 |
| D、Na2CO3不能转化成NaHCO3,而NaHCO3能转化成Na2CO3 |
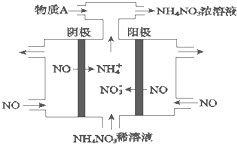 (1)室温下,向Na2S的水溶液中加入等体积等浓度的盐酸,反应后所得的溶液中,除氢离子之外的离子浓度由小到大的顺序为:
(1)室温下,向Na2S的水溶液中加入等体积等浓度的盐酸,反应后所得的溶液中,除氢离子之外的离子浓度由小到大的顺序为: