题目内容
取1.43g Na2CO3·10H2O溶于水配成100ml溶液,求:(要求写出计算过程)
(1)Na2CO3物质的量浓度;
(2)Na+ 物质的量浓度;
(3)取出20ml该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.04mol/L,求加入蒸馏水的体积(设稀释时,对溶液体积的影响忽略不计)。
(1)0.05mol/L;(2)0.1mol/L;(3)5mL
【解析】
试题分析:(1)n(Na2CO3)= 1.43g÷286g/mol=0.005mol, c(Na2CO3)= n(Na2CO3)÷V=0.005mol÷0.1L=0.05mol/L;(2)c(Na+)= 2c(Na2CO3)=0.1mol/L;(3)在溶液稀释过程中溶质的物质的量不变,所以若取出20ml该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.04mol/L,则稀释后溶液的体积是V=(0.05 mol/L×20ml)÷0.04mol/L=25ml。稀释时,对溶液体积的影响忽略不计,所以求加入蒸馏水的体积是25ml-20ml=5ml。
考点:考查溶液的物质的量浓度计算、电解质的浓度与电离产生的离子浓度的关系、物质的量浓度的溶液的稀释的知识。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
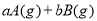
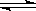
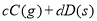
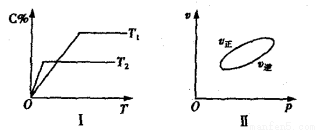
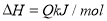 ,反应过程中,当其他条件不变时,C在混合物中的含量与温度(T)的关系如图I所示,反应速率(v)与压强(p)的关系如图II所示。据图分析,以下说法正确的是( )
,反应过程中,当其他条件不变时,C在混合物中的含量与温度(T)的关系如图I所示,反应速率(v)与压强(p)的关系如图II所示。据图分析,以下说法正确的是( )