题目内容
将一定量的晶体A,隔绝空气加热到200℃时,A全部分解为等物质的量的四种气体.这四种物质与其他的相互转化关系如图所示.F和J是中学化学中常见的两种单质.H为红棕色气体.图中部分反应条件及生成物没有列出.请按要求填空:

(1)单质F的化学式
(2)写出B和F反应的化学方程式 ,L和B的水溶液反应的离子方程式 ;
(3)写出K与I的稀溶液反应的离子方程式
(4)A的化学式为
(5)工业上以硫酸亚铁、稀硫酸和亚硝酸钠为原料来制备某高效净水剂Fe(OH)SO4,反应有G生成,该反应的化学方程式是 .

(1)单质F的化学式
(2)写出B和F反应的化学方程式
(3)写出K与I的稀溶液反应的离子方程式
(4)A的化学式为
(5)工业上以硫酸亚铁、稀硫酸和亚硝酸钠为原料来制备某高效净水剂Fe(OH)SO4,反应有G生成,该反应的化学方程式是
考点:无机物的推断
专题:推断题
分析:H为红棕色气体,则H为NO2,F和J是中学化学中常见的两种单质,且F由过氧化钠与C反应的产物,所以F为O2,则G为NO,B可与氧气在催化剂条件下加热反应得到G与D,B能与氧气继续反应,则B为NH3,D为H2O,则C为CO2,I为HNO3.L与B反应得到红褐色沉淀为Fe(OH)3,D(H2O)与J在高温下反应,结合转化关系,根据Fe元素守恒可知,J为Fe,K为Fe3O4,L为Fe(NO3)3,E可K与反应生成Fe和CO2,则E具有还原性,应为CO,晶体A隔绝空气加热到200°C时,全部分解为B、C、D、E四种气体,且其物质的量相等,则A应为NH4HC2O4,据此答题;
解答:
解:H为红棕色气体,则H为NO2,F和J是中学化学中常见的两种单质,且F由过氧化钠与C反应的产物,所以F为O2,则G为NO,B可与氧气在催化剂条件下加热反应得到G与D,B能与氧气继续反应,则B为NH3,D为H2O,则C为CO2,I为HNO3.L与B反应得到红褐色沉淀为Fe(OH)3,D(H2O)与J在高温下反应,结合转化关系,根据Fe元素守恒可知,J为Fe,K为Fe3O4,L为Fe(NO3)3,E可K与反应生成Fe和CO2,则E具有还原性,应为CO,晶体A隔绝空气加热到200°C时,全部分解为B、C、D、E四种气体,且其物质的量相等,则A应为NH4HC2O4,
(1)根据上面的分析可知,单质F的化学式为O2,
故答案为:O2;
(2)B和F反应的化学方程式为4NH3+5O2
4NO+6H2O,L和B的水溶液反应的离子方程式为Fe3++3NH3?H2O=3NH4++Fe(OH)3↓,
故答案为:4NH3+5O2
4NO+6H2O;Fe3++3NH3?H2O=3NH4++Fe(OH)3↓;
(3)K与I的稀溶液反应的离子方程式为3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O,
故答案为:3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O;
(4)根据上面的分析可知,A的化学式为NH4HC2O4,
故答案为:NH4HC2O4;
(5)工业上以硫酸亚铁、稀硫酸和亚硝酸钠为原料来制备某高效净水剂Fe(OH)SO4,反应有G生成,该反应的化学方程式是2FeSO4+2NaNO2+H2SO4=2Fe(OH)SO4+Na2SO4+2NO↑,
故答案为:2FeSO4+2NaNO2+H2SO4=2Fe(OH)SO4+Na2SO4+2NO↑;
(1)根据上面的分析可知,单质F的化学式为O2,
故答案为:O2;
(2)B和F反应的化学方程式为4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
(3)K与I的稀溶液反应的离子方程式为3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O,
故答案为:3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O;
(4)根据上面的分析可知,A的化学式为NH4HC2O4,
故答案为:NH4HC2O4;
(5)工业上以硫酸亚铁、稀硫酸和亚硝酸钠为原料来制备某高效净水剂Fe(OH)SO4,反应有G生成,该反应的化学方程式是2FeSO4+2NaNO2+H2SO4=2Fe(OH)SO4+Na2SO4+2NO↑,
故答案为:2FeSO4+2NaNO2+H2SO4=2Fe(OH)SO4+Na2SO4+2NO↑;
点评:本题考查无机物的推断,题目突破口较少,且不明显,需要学生熟练掌握元素化合物知识,侧重于学生的分析能力和元素化合物知识的综合运用,注意根据物质的颜色、状态及特殊的转化关系为突破口进行推断,难度较大.

练习册系列答案
相关题目
常温下,在溶液中可发生以下反应:①2Fe2++Br2═2Fe3++2Br-,②2Br-+Cl2═Br2+2Cl-,③2Fe3++2I-═2Fe2++I2;下列说法错误的是( )
| A、铁元素在反应①和③中均被氧化 |
| B、反应②中当有1mol Cl2被还原时,有2mol Br-被氧化 |
| C、氧化性强弱顺序为:Cl2>Br2>Fe3+>I2 |
| D、还原性强弱顺序为:I->Fe2+>Br->Cl- |
在无色酸性溶液中,可以大量共存的离子组是( )
| A、NH4+、NO3-、Cl-、S2- |
| B、K+、HCO3-、MnO4-、SO42- |
| C、NH4+、NO3-、Cl-、K+ |
| D、NH4+、Fe3+、Cl-、I- |
下列叙述涉及的化学相关知识,其中说法正确的是( )
| A、植物油可以作为萃取剂分离出碘水中的碘 |
| B、石油的分馏、煤的气化、海水制镁都包括化学变化 |
| C、处理废水时加入明矾作为消毒剂,可以除去水中的杂质 |
| D、乙烯、甲烷、SO2三种无色气体可用溴水鉴别 |
从海带中制取单质碘需要经过灼烧、溶解、过滤、氧化、萃取、分液、蒸馏等操作.下列图示对应的装置合理、操作规范的是( )
A、 灼烧 |
B、 过滤 |
C、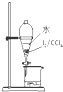 分液 |
D、 蒸馏 |

 某离子晶体的晶胞结构如图所示,X(●)位于立方体的顶点,Y(○)位于立方体的中心,试分析:
某离子晶体的晶胞结构如图所示,X(●)位于立方体的顶点,Y(○)位于立方体的中心,试分析: