题目内容
4.下列指定微粒的数目相等的是( )| A. | 等物质的量的CaCl2和CaO2含有的离子数 | |
| B. | 等温等压下,质子数相等的CO、N2、C2H2三种气体含有的原子数 | |
| C. | 同温、同压、同体积的CO和NO含有的质子数 | |
| D. | 物质的量相同的铁和铝分别与足量氯气完全反应时转移的电子数 |
分析 A.1mol氯化钙中含有3mol离子,1mol CaO2中含有含有2mol离子;
B.CO、N2、C2H2中都含有14个质子,其分子中含有的原子数不相等;
C.同温、同压、同体积的CO和NO物质的量相等,二者含有的质子数不相等;
D.Fe、Al与氯气分别生成氯化铁、氯化铝,产物中金属元素的化合价都是+3价,根据电子守恒分析.
解答 解:A.1molCaCl2中含有1mol钙离子、2mol氯离子,总共含有3mol离子,而1molCaO2中含有1mol钙离子和1mol过氧根离子,总共含有2mol离子,所以等物质的量的CaCl2和CaO2含有的离子数不相等,故A错误;
B.质子数相等的CO、N2、C2H2三种气体的物质的量相等,由于其分子中含有的原子数不相等,则含有的原子数不相等,故B错误;
C.同温、同压、同体积的CO和NO的物质的量相等,由于二者含有的质子数不相等,则含有的质子数不同,故C错误;
D.物质的量相同的铁和铝分别与足量氯气完全反应,由于产物中金属元素化合价都是+3价,则反应过程中转移的电子数一定相等,故D正确;
故选D.
点评 本题考查了物质的量的计算,题目难度中等,明确物质的量与气体摩尔体积、摩尔质量、阿伏伽德罗常数之间的关系即可解答,A为易错点,注意CaO2中的阴离子为过氧根离子.

练习册系列答案
相关题目
1.下列有关说法错误的是( )
| A. | 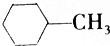 的一氯代物最多有4种 的一氯代物最多有4种 | |
| B. | 乙酸可与乙醇、金属钠、新制Cu(OH)2悬浊液等物质反应 | |
| C. | Cl2可与乙烷发生取代反应,与乙烯发生加成反应 | |
| D. | 阿托酸(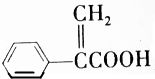 )可用于合成高分子材料 )可用于合成高分子材料 |
9.下表为元素周期表的一部分.
回答下列问题:
(1)Z元素在周期表中的位置为第三周期,第ⅤⅡA族.
(2)表中元素原子半径最大的是(写元素符号)Si.
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是ac.
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,烃的电子式为 .Q与水反应的化学方程式为Mg2C3+4H2O=2Mg(OH)2+C3H4↑.
.Q与水反应的化学方程式为Mg2C3+4H2O=2Mg(OH)2+C3H4↑.
(5)X与Z两元素的单质反应生成1molX的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程
式Si(s)+2Cl2(g)=SiCl4(l)△H=-687kJ/mol.
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种元素组成,气体的相对分子质量都小于50.为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/LNaOH溶液和1molO2,则两种气体的分子式及物质的量分别为NO 0.9mol,NO2 1.3mol,生成硫酸铜物质的量为2mol.
| 碳 | 氮 | Y | |
| X | 硫 | Z |
(1)Z元素在周期表中的位置为第三周期,第ⅤⅡA族.
(2)表中元素原子半径最大的是(写元素符号)Si.
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是ac.
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,烃的电子式为
 .Q与水反应的化学方程式为Mg2C3+4H2O=2Mg(OH)2+C3H4↑.
.Q与水反应的化学方程式为Mg2C3+4H2O=2Mg(OH)2+C3H4↑.(5)X与Z两元素的单质反应生成1molX的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程
式Si(s)+2Cl2(g)=SiCl4(l)△H=-687kJ/mol.
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种元素组成,气体的相对分子质量都小于50.为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/LNaOH溶液和1molO2,则两种气体的分子式及物质的量分别为NO 0.9mol,NO2 1.3mol,生成硫酸铜物质的量为2mol.
 .
. .
. .
. ,元素D在元素周期表中的位置是第三周期VIIA族.
,元素D在元素周期表中的位置是第三周期VIIA族.