题目内容
1.(1)为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1mol CO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
T温度下,测得CO2和CH3OH(g)的浓度随时间变化如下图.请回答下列问题:
①达平衡时,氢气的平衡浓度为C (H2)=0.75mol/L.
②能够说明该反应已达到平衡的是AC(填字母序号,下同).
A.恒温、恒容时,容器内的压强不再变化
B.恒温、恒容时,容器内混合气体的密度不再变化
C.一定条件下,CO、H2和CH3OH的浓度保持不变
D.一定条件下,单位时间内消耗3mol H2的同时生成1mol CH3OH
③下列措施中能使平衡混合物中$\frac{{n(C{H_3}OH)}}{{n(C{O_2})}}$增大的是CD.
A.加入催化剂 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.降低温度
④求此温度(T)下该反应的平衡常数K=$\frac{16}{3}$.若开始时向该1L密闭容器中充入1mol CO2,2molH2,1.5mol CH3OH和1mol H2O(g),则反应向正(填“正”或“逆”)反应方向进行.
(2 )汽车燃油不完全燃烧时产生CO,在汽车中装置催化转化器可减少CO和NO的污染,其化学反应方程式为2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2.
分析 (1)①由图可知,10min到达平衡,平衡时甲醇的浓度变化为0.75mol/L,由方程式可知氢气的浓度变化等于甲醇的浓度变化量3倍为2.25mol/L;
②可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析解答;
③要使$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大,应使平衡向正反应方向移动;
④K为生成物浓度幂之积与反应物浓度幂之积的比,结合平衡浓度计算;
(2)根据生成物为氮气和二氧化碳书写.
解答 解:(1)①由图可知,10min到达平衡,平衡时甲醇的浓度变化为0.75mol/L,由方程式CO2(g)+3H2(g)?CH3OH(g)+H2O可知,氢气的浓度变化等于甲醇的浓度变化量为0.75mol/L×3=2.25mol/L,故氢气的平衡浓度c(H2)=3mol/L-2.25mol/L=0.75mol/(L•mon),
故答案为:0.75;
②A.反应前后气体的体积不等,所以压强一直在变,则当压强不变时能说明达到平衡,故A正确;
B.反应前后质量不变,体积也不变,所以密度一直不变,则混合气体的密度不再变化不能说明达到平衡,故B错误;
C.CO2、H2和CH3OH的浓度不再变化,说明达到平衡,故C正确;
D.单位时间内消耗3molH2的同时生成1molCH3OH,都是指正反应方向,不能说明达到平衡,故D错误;
故选AC;
③要使$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大,应使平衡向正反应方向移动,
A.因正反应放热,升高温度平衡向逆反应方向移动,则$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$减小,故A错误;
B.充入He(g),使体系压强增大,但对反应物质来说,浓度没有变化,平衡不移动,$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$不变,故B错误;
C.将H2O(g)从体系中分离,平衡向正反应方法移动,$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大,故C正确;
D.再充入1mol CO2和3mol H2,等效于在原来基础上缩小体积一半,压强增大,平衡向正反应方向移动,则$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大,故D正确;
故答案为:CD;
④K为生成物浓度幂之积与反应物浓度幂之积的比,则K=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$,
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
开始 1 3 0
转化 0.75 2.25 0.75 0.75
平衡 0.25 0.75 0.75 0.75
体积为1L的密闭容器,平衡浓度分别为0.25mol/L、0.75mol/L、0.75mol/L、0.75mol/L,
K=$\frac{0.75×0.75}{0.25×(0.75)^{3}}$=$\frac{16}{3}$,
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
开始 1 2 1.5 1
则Q=$\frac{1.5×1}{1×{2}^{3}}$<$\frac{16}{3}$=K,故正向进行,
故答案为:K=$\frac{16}{3}$;正;
(2)汽车尾气系统中装置反应的化学方程式为2CO+2NO $\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2,
故答案为:2CO+2NO $\frac{\underline{\;催化剂\;}}{\;}$ 2CO2+N2.
点评 考查反应速率计算、化学平衡的计算与影响因素、平衡常数等,难度中等,注意基础知识的掌握.

 天天练口算系列答案
天天练口算系列答案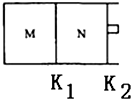 恒温下,向一个4L的密闭容器中充入5.2molH2和2molN2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:
恒温下,向一个4L的密闭容器中充入5.2molH2和2molN2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol•L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
A.N2、H2和NH3的浓度不再变化
B.单位时间内消耗n mol N2同时消耗3nmol H2
C.1mol氮氮三键断裂同时6molN-H键断裂
D.容器内总压强不随时间而变化
E.混合气体的密度保持不变
F.混合气体的平均相对分子质量不再改变
②此条件下该反应的化学平衡常数K=0.1,若温度不变,只将容器体积由4L变为2L,达到新平衡时N2的平衡浓度>0.4mol•L-1(填“>”、“=”或“<”).
③如图所示,隔板K1固定不动,活塞K2可自由移动.T℃时,M、N两个容器中均发生反应N2(g)+3H2(g)?2NH3(g),向容器M、N中各充入l mol N2和3mol H2,初始M、N的容积和温度相同,并保持温度不变.下列有关说法中不正确的是A.
A.反应达到平衡时N2的转化率:M>N
B.H2的体积分数:M>N
C.容器N中达到平衡,测得容器中含有1.2mol NH3,此时N的容积为VL,则该反应在此条件下的平衡常数K=
$\frac{24{V}^{2}}{12}$
D.该反应在T℃时的平衡常数K:M=N.
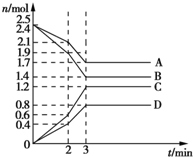 在某容积为2L的密闭容器中,A、B、C、D四种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变化如图所示.下列说法正确的是( )
在某容积为2L的密闭容器中,A、B、C、D四种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变化如图所示.下列说法正确的是( )| A. | 前2min内,v(A)=0.2 mol/(L•min) | |
| B. | 在2min时,图象发生改变的原因只可能是增大压强 | |
| C. | 其他条件不变,3min时体系的压强不再发生变化 | |
| D. | 增加气体D的浓度,A的反应速率随之减小 |
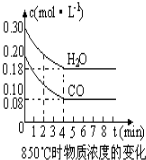 在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0,CO和H2O浓度变化如图.
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0,CO和H2O浓度变化如图.t℃时物质浓度(mol•L-1)的变化:
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
(2)850℃时,此反应的平衡常数K=1,若保持温度、体积不变,起始时CO和H2O的浓度均为0.2mol•L-1,则达平衡时CO的转化率为50%.在850℃时,若上述反应体系中各物质浓度为C(CO)=0.07mol•L-1C(H2O)=0.17mol•L-1C( CO2)=0.13mol•L-1C(H2)=0.13mol•L-1,则此时该反应向逆方向移动.
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表.
①表中3min~4min之间反应处于平衡状态; c 1数值大于0.08mol•L-1 (填大于、小于或等于)
②反应在4min~5min间,平衡向逆方向移动,可能的原因是d (单选),表中5min~6min之间数值发生变化,可能的原因是a (单选)
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
| A. | 硫化锌转化成铜蓝的离子方程式为ZnS(s)+Cu2+(aq)=Zn2+(aq)+CuS(s) | |
| B. | 在白色硫化锌浊液中滴加硝酸铅溶液,不会生成黑色沉淀(PbS) | |
| C. | 在水中的溶解度:S(ZnS)>S(PbS)>S(CuS) | |
| D. | 若溶液中c(Cu2+)=1×10-10mol•L-1,则S2-已完全转化成CuS |
| A. | Na2CO3 | B. | NaOH | C. | Mg(OH)2 | D. | NH3•H2O |
| A. | 固体氯化钠 | B. | 液态氯化氢 | C. | 乙醇溶液 | D. | 液态氢氧化钾 |
| A. | 在电解池中,物质在阴极发生氧化反应 | |
| B. | 在电解池中,与电源正极相连的电极是阴极 | |
| C. | 在原电池中,物质在负极发生氧化反应 | |
| D. | 在原电池中,电子由正极流向负极 |
 2NH3(g)△H=-92kJ•mol-1.
2NH3(g)△H=-92kJ•mol-1.