题目内容
亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。

(1)双氧水的电子式为 ;Ⅰ中发生反应的还原剂是 (填化学式)。
(2)Ⅱ中反应的离子方程式是 。
(3)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备。
①写出该反应的化学方程式: ;
②研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析,其原因是 。
(4)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量 (填“相同”、“不相同”或“无法判断”)
(10分)(1) 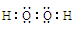 Na2SO3 (2)2ClO2 + H2O2 + 2OH-=2ClO2-+ O2↑+ 2H2O
Na2SO3 (2)2ClO2 + H2O2 + 2OH-=2ClO2-+ O2↑+ 2H2O
(3) ① 5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O ②ClO2-的氧化性或Cl-的还原性随溶液的酸性和浓度的增大而增强,因此Cl-被氧化得到Cl2 (4)相同
【解析】
试题分析:(1)双氧水是含有极性键和非极性键的共价化合物,其电子式为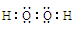 。反应I中氯酸钠转化为ClO2,亚氯酸钠转化为硫酸钠,其中氯元素的化合价降低,S元素的化合价升高,则还原剂是Na2SO3。
。反应I中氯酸钠转化为ClO2,亚氯酸钠转化为硫酸钠,其中氯元素的化合价降低,S元素的化合价升高,则还原剂是Na2SO3。
(2)ClO2与双氧水反应生成亚氯酸钠,其中氯元素的化合价降低,则双氧水被氧化,所以气体a是氧气,则反应的离子方程式为2ClO2+H2O2+2OH-=2ClO2-+O2↑+ 2H2O。
(3)①亚氯酸钠和稀盐酸为原料制备ClO2,根据亚氯酸钠中氯元素的化合价为+3甲可知亚氯酸钠应该既是氧化剂,也是还原剂,则反应的化学方程式为5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O。
②由于ClO2-的氧化性或Cl-的还原性随溶液的酸性和浓度的增大而增强,因此在反应中Cl-被氧化得到Cl2。
(4)由于不论是亚氯酸钠,还是氯酸钠与硫酸亚铁反应时,均被还原为氯化钠,因此足量FeSO4溶液反应时根据电子得失守恒可知消耗Fe2+的物质的量相同。
考点:考查物质制备工艺流程图的分析与应用

 阅读快车系列答案
阅读快车系列答案已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是:

选项 | A | B | C | D |
X | C | Fe | Ca(OH)2溶液 | AlCl3 |
W | O2 | HNO3 | CO2 | NH3·H2O |
(14分)A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。
(1)A在周期表位置________写出一种工业制备单质F的离子方程式:___________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为_______其水溶液与F单质反应的化学方程式为__________________________________.
(3)由这些元素组成的物质,其组成和结构信息如下表:
物质 | 组成和结构信息 |
a | 含有A的二元离子化合物 |
b | 含有非极性共价键的二元离子化合物,且原子数之比为1∶1 |
c | 化学组成为BDF2 |
d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式为________;b的化学式为______________;
c的电子式为________, d是________晶体
(4)由A和B元素组成的二元化合物是 沼气的主要成分,其与氧气在酸性电解质溶液中组成燃料电池消耗标况下11.2L氧气时转移电子数为__________mol。


 pC(g)+qQ(g) 当m、n、p、q为任意整数时,达到平衡的标志是
pC(g)+qQ(g) 当m、n、p、q为任意整数时,达到平衡的标志是