��Ŀ����
29.�������Ļ�����Ӧ�ù㷺.��FeCl3������������ӡˢ��·ͭ�帯ʴ��������ֹѪ���ȡ�(1)д��FeCl3��Һ��ʴӡˢ��·ͭ������ӷ���ʽ_______________________________��
(2)����(1)�еķ�Ӧ��Ƴ�ԭ��أ��뻭��ԭ��ص�װ��ͼ�����������������д���缫��Ӧʽ��
������Ӧ___________________ ������Ӧ________________________
(3)��ʴͭ���Ļ����Һ�У���Cu2+��Fe3+��Fe2+��Ũ�Ⱦ�Ϊ0.10mol��L-1��������±����������ݺ�ҩƷ��������ȥCuCl2��Һ��Fe3+��Fe2+��ʵ�鲽��__________________________��
| �������↑ʼ����ʱ��pH | �������������ȫʱԼpH |
Fe3+ Fe2+ Cu2+ | 1.9 7.0 4.7 | 3.2 9.0 6.7 |
�ṩ��ҩƷ��Cl2 ŨH2SO4 NaOH��Һ CuO Cu | ||
(4)ij������Ա�������ʲ���������и�ʴ����������ijЩ����Һ�и�ʴ�������ԡ�����ϱ��ṩ��ҩƷ��ѡ������(ˮ����ѡ)��������ʵ�飬��֤���ʲ�����ױ���ʴ��
�йط�Ӧ�Ļ�ѧ����ʽ__________________________
���ʲ���ָ�ʴ��ʵ������_________________________________
(1)2Fe3++Cu=2Fe2++Cu2+
(2)װ��ͼ
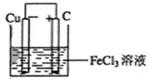
������Ӧ��Fe3++e-=Fe2+(��2Fe3++2e-=2Fe2+)
������Ӧ��Cu=Cu2++2e-(��Cu-2e-=Cu2+)
(3)��ͨ������������Fe2+������Fe3+;�ڼ���CuO������Һ��pH��3.2��4.7��
�۹���(��ȥFe(OH)3)
(4)CuO+H2SO4=CuSO4+H2O
CuSO4+Fe=FeSO4+Cu
����ֱ������Ϻ�ɫ��������
���������⿼��绯ѧ�����Ļ������֪ʶ����Cu��FeCl3��Һ��Ӧ���Ϊԭ��أ�Cu�����������Ե缫ʯī��������FeCl3��ҺΪ�������Һ����ȥ��Cu2+����Һ�е�Fe3+��Fe2+���Ȱ�Fe2+����ΪFe3+���ɱ��������ɼ�CuO��pH 3.2��4.7��ʹFe3+ת��ΪFe(OH)3��������ȥ���ɲ���������в��ױ���ʴ����ijЩ�����ױ���ʴ��ȡ����CuO����������H2SO4�Ƴ�CuSO4��Һ��ȡ����ַ���CuSO4��Һ��������ֱ����к�ɫ���ʳ��֣�֤���ױ�����Һ��ʴ��

 ��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�