题目内容
13.氨气的电子式 ;
;17号元素阴离子的电子式
 .
.
分析 N原子的最外层有5个电子,其中3个未成对电子和1对成对电子;
17号元素阴离子即Cl-,氯离子为阴离子,电子式中需要标出最外层所带电荷.
解答 解:N原子的最外层有5个电子,其中3个未成对电子和1对成对电子,3个未成对电子分别和3个H原子形成3对共用电子对,故氨气的电子式为 ;
;
第17号元素为氯元素,其阴离子为氯离子,由于氯离子为阴离子,电子式中需要标出其最外层电子,氯离子正确的电子式为: .
.
故答案为: ;
; .
.
点评 本题考查了常见物质和离子的电子式的书写,难度不大,应注意的是书写阴离子的电子式时应标出最外层电子.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
1.常温下,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1mol•L-1pH为4的NaHA溶液中:c(HA-)>c(H2A)>c(A2-) | |
| B. | 向饱和氯水中加入NaOH溶液至pH=7,所得溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(OH-) | |
| C. | 0.10mol•L-1 KHC2O4溶液中:c(OH-)=c(H+)+c(H2C2O4)-c(C2O42-) | |
| D. | 0.10mol•L-1Na2SO3溶液通入少量SO2:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)] |
8.10ml浓度为1mol/L的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成的是( )
| A. | KOH | B. | CH3COONa | C. | CuSO4 | D. | Na2CO3 |
18.质子数≤18的A和M两种元素,已知A2-与M+的电子数之差为8,则下列说法正确的是( )
| A. | A和M原子的最外层电子数之差不一定为5 | |
| B. | A和M原子的最外层电子数之和一定为7 | |
| C. | A和M原子的电子数之差一定为11 | |
| D. | A和M的原子序数之差不一定为5 |
5.下列叙述中,正确的是( )
| A. | 两种粒子,若核外电子排布完全相同,则其化学性质相同 | |
| B. | 凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 | |
| C. | 一种微粒与另一种微粒的质子数和电子数均相等,它们可能是一种离子和一种分子 | |
| D. | 不存在两种质子数和电子数均相同的阳离子和阴离子 |
2.下列物质中含有官能团种类最多的是( )
| A. | 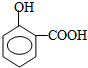 | B. | 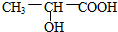 | ||
| C. | 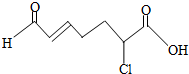 | D. | CH2OH(CHOH)4CHO |
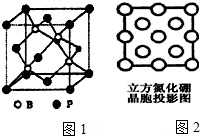 由N、B等元素组成的新型材料有着广泛用途.
由N、B等元素组成的新型材料有着广泛用途.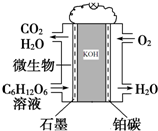 微生物燃料电池是利用微生物作为反应主体,将有机物的化学能转化为电能.如以葡萄糖溶液为例,其工作原理如图所示:
微生物燃料电池是利用微生物作为反应主体,将有机物的化学能转化为电能.如以葡萄糖溶液为例,其工作原理如图所示: