题目内容
一定温度下,在2L密闭容器中发生下列反应:4NO2(g)+O2(g) 2N2O5(g);已知该反应的平衡常数:
2N2O5(g);已知该反应的平衡常数: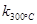 >
>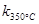 ,且体系中
,且体系中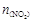 (单位:mol)随时间变化如下表:
(单位:mol)随时间变化如下表:
|
时间(s) |
0 |
500 |
1000 |
1500 |
|
t1℃ |
20 |
13.96 |
10.08 |
10.08 |
|
t2℃ |
20 |
a |
b |
c |
下列说法一定正确的是
A.正反应为吸热反应
B.如果t2℃<t1℃,那么 a>b=c,且a=10+0.5b
C.如果t2℃<t1℃,那么t2℃达到平衡的时间介于1000s至1500s之间
D.如果t2℃>t1℃,那么b>10.08
【答案】
D
【解析】
试题分析:A、K300℃>K350℃知温度越高K越小,正反应为放热反应,正确;B、温度降低在1000-1500间不一定建立平衡,b≠c,错误;C、温度降低,到达平衡时间增长,但无法确定具体的时间,错误;D、放热反应,温度升高,反应物转化率降低,正确。
考点:考查化学实验速率、平衡相关知识。

练习册系列答案
相关题目