题目内容
某研究性学习小组在网上收集到如下信息:钾、钙、钠、镁等活泼金属都能在CO2气体中燃烧.他们对钠在CO2气体中燃烧后的产物中的白色物质进行了如下探究:
【实验】将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质.
【提出假设】假设1:白色物质是Na2O.
假设2:白色物质是Na2CO3.
假设3: (请你写出).
【设计实验方案、验证假设】该小组对燃烧后的白色产物进行如下探究:
【思考与交流】
(1)甲同学认为方案1得到的结论不正确,其理由是 .
(2)通过方案1和方案2的实验,你认为上述三个假设中, 成立.你的理由是 .
(3)钠在二氧化碳中燃烧的化学方程式为 .
(4)乙同学认为白色物质有可能是氢氧化钠.你是否同意乙同学的观点,并简述由: .
【实验】将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质.
【提出假设】假设1:白色物质是Na2O.
假设2:白色物质是Na2CO3.
假设3:
【设计实验方案、验证假设】该小组对燃烧后的白色产物进行如下探究:
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | (此处不要求填写) |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
(1)甲同学认为方案1得到的结论不正确,其理由是
(2)通过方案1和方案2的实验,你认为上述三个假设中,
(3)钠在二氧化碳中燃烧的化学方程式为
(4)乙同学认为白色物质有可能是氢氧化钠.你是否同意乙同学的观点,并简述由:
考点:物质的检验和鉴别的实验方案设计
专题:实验设计题
分析:钠在二氧化碳中燃烧生成的白色固体可能为Na2O、Na2CO3或Na2O和 Na2CO3混合物;
(1)碳酸钠溶液水解呈碱性,氧化钠溶于水反应生成氢氧化钠溶液呈碱性;
(2)依据方案①②的反应现象和结论综合分析判断;假设2符合反应现象,溶于水溶液呈碱性,加入过量氯化钙沉淀后的溶液遇酚酞不变色证明不含氧化钠;
(3)依据方案①②的反应现象和结论,分析和推断钠在二氧化碳中燃烧生成碳酸钠和碳;
(4)依据反应物中的元素守恒分析判断生成物的组成元素.
(1)碳酸钠溶液水解呈碱性,氧化钠溶于水反应生成氢氧化钠溶液呈碱性;
(2)依据方案①②的反应现象和结论综合分析判断;假设2符合反应现象,溶于水溶液呈碱性,加入过量氯化钙沉淀后的溶液遇酚酞不变色证明不含氧化钠;
(3)依据方案①②的反应现象和结论,分析和推断钠在二氧化碳中燃烧生成碳酸钠和碳;
(4)依据反应物中的元素守恒分析判断生成物的组成元素.
解答:
解:钠在二氧化碳中燃烧生成的白色固体可能为Na2O、Na2CO3或Na2O和 Na2CO3混合物,故答案为:白色物质是Na2O和 Na2CO3混合物;
(1)取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液溶液变红,原因有,可以是生成的氧化钠溶于水和水反应生成氢氧化钠溶液的作用,也可以碳酸钠溶液水解显碱性的作用,也可以是二者的混合物,所以方案1不正确,
故答案为:Na2CO3溶液显碱性,也会使酚酞变红;
(2)依据上述分析和现象判断,假设2正确;因为取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液,出现白色沉淀,说明含有碳酸钠,静置片刻,取上层清液于试管中,滴加无色酚酞试液无变化,说明一定无氧化钠,因为氧化钠和水反应一定生成氢氧化钠溶液,
故答案为:假设2;方案2①中出现的白色沉淀是CaCO3,所以燃烧后的白色产物中Na2CO3存在;方案2②中滴加无色酚酞试液无明显现象,说明燃烧后的白色产物中没有Na2O存在;
(3)依据现象和实验分析判断钠在二氧化碳气体中燃烧生成碳酸钠和碳单质,反应的化学方程式为:4Na+3CO2
2Na2CO3+C,
故答案为:4Na+3CO2
2Na2CO3+C;
(4)丙同学认为白色物质有可能是氢氧化钠.是错误的,在反应过程中,是钠在二氧化碳气体中 的燃烧反应,无氢元素的存在,实验依据元素守恒可置换不可能生成氢氧化钠,
故答案为:不同意,因为反应物中无氢元素(或违背质量守恒定律).
(1)取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液溶液变红,原因有,可以是生成的氧化钠溶于水和水反应生成氢氧化钠溶液的作用,也可以碳酸钠溶液水解显碱性的作用,也可以是二者的混合物,所以方案1不正确,
故答案为:Na2CO3溶液显碱性,也会使酚酞变红;
(2)依据上述分析和现象判断,假设2正确;因为取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液,出现白色沉淀,说明含有碳酸钠,静置片刻,取上层清液于试管中,滴加无色酚酞试液无变化,说明一定无氧化钠,因为氧化钠和水反应一定生成氢氧化钠溶液,
故答案为:假设2;方案2①中出现的白色沉淀是CaCO3,所以燃烧后的白色产物中Na2CO3存在;方案2②中滴加无色酚酞试液无明显现象,说明燃烧后的白色产物中没有Na2O存在;
(3)依据现象和实验分析判断钠在二氧化碳气体中燃烧生成碳酸钠和碳单质,反应的化学方程式为:4Na+3CO2
| ||
故答案为:4Na+3CO2
| ||
(4)丙同学认为白色物质有可能是氢氧化钠.是错误的,在反应过程中,是钠在二氧化碳气体中 的燃烧反应,无氢元素的存在,实验依据元素守恒可置换不可能生成氢氧化钠,
故答案为:不同意,因为反应物中无氢元素(或违背质量守恒定律).
点评:本题考查物质的组成探究,为高频考点,侧重于学生的分析能力和实验能力的考查,注重于物质性质的综合应用,反应现象的分析判断,反应产物的分析判断,实验现象是解题判断的关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:下列说法不正确的是( )
| T/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A、反应前2 min的平均速率v(Z)=2.0×10-3mol/(L?min) |
| B、其他条件不变,升高温度,反应达到新平衡前v(逆)>v (正) |
| C、该温度下此反应的平衡常数K=1.44 |
| D、其他条件不变,再充入0.2 mol Z,平衡时X的体积分数不变 |
下列方程式正确的是( )
A、用铁丝网作电极,电解饱和食盐水:2Cl-+2H2O
| ||
| B、Ba(OH)2溶液中加入过量的Al2(SO4)3溶液:3Ba2++6OH-+2Al3++3SO42-→3BaSO4↓+2Al(OH)3↓ | ||
| C、向H218O中投入Na2O2固体:2H218O+2Na2O2→4Na++4OH-+18O2↑ | ||
| D、石灰乳中Ca(OH)2的电离:Ca(OH)2(s)?Ca2++2OH- |
设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A、0.1 mol?L-1的NaHCO3 溶液中含有Na+的数目为0.1NA |
| B、标准状况下,1mol苯含有C=C 双键的数目为3NA |
| C、常温常压下,14 g 由N2与CO组成的混合气体含有的原子数目为NA |
| D、标准状况下,22.4L NO2与水充分反应转移的电子数目为0.1NA |
设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、含4.8g 碳元素的石墨晶体中的共价键数是0.8NA |
| B、标准状况下,11.2LCO和N2的混合气体中,含有的原子数为NA |
| C、1mol的羟基(-OH)与1mol的氢氧根离子(OH-)所含电子数均为9NA |
| D、常压、500℃、催化条件下,1molSO2和0.5molO2充入一密闭容器内,充分反 应后的生成物分子数为NA |

 ),而且原子利用率为100%,为绿色化学,写出反应方程式
),而且原子利用率为100%,为绿色化学,写出反应方程式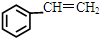 可被氧化剂氧化生成
可被氧化剂氧化生成  、HCOOH和H2O,该氧化剂为:
、HCOOH和H2O,该氧化剂为: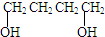 和2mol乙酸在浓硫酸作用下生成分子式为C8H14O4的酯,写出反应方程式:
和2mol乙酸在浓硫酸作用下生成分子式为C8H14O4的酯,写出反应方程式: