题目内容
7.如图表示一定条件下反应N2(g)+3H2(g)?2NH3(g)△H<0的反应速率与反应过程的曲线关系图.下列说法正确的是( )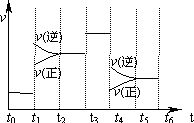
| A. | t2~t3和t3~t4时间段氨气的体积分数相等 | |
| B. | 氨气的体积分数最高的一段时间为t5~t6 | |
| C. | t4时刻改变的条件是降低温度 | |
| D. | t4~t5时间段平衡向正反应方向移动 |
分析 该反应为气体体积减小的反应,且为放热反应,由图象可知,t1时正逆反应速率均增大,且逆反应速率大于正反应速率,则平衡逆向移动;t3时正逆反应速率同等程度的增大,t4时正逆反应速率均减小,但逆反应速率大于正反应速率,则化学平衡逆向移动,以此来解答.
解答 解:该反应为气体体积减小的反应,且为放热反应,由图象可知,t1时正逆反应速率均增大,且逆反应速率大于正反应速率,则平衡逆向移动;t3时正逆反应速率同等程度的增大,t4时正逆反应速率均减小,但逆反应速率大于正反应速率,则化学平衡逆向移动,
A.t2-t3达到化学平衡状态,体积分数不变,t3-t4时间段化学平衡不移动,所以氨气的体积分数相等,故A正确;
B.由上述分析可知,t3时平衡不移动,t1、t4时改变条件反应均逆向移动,氨气的含量减少,则氨气的体积分数最高的一段时间为t0-t1,故B错误;
C.t4时正逆反应速率均减小,且逆反应速率大于正反应速率,平衡逆向移动,改变条件为降低压强,而降低温度平衡正向移动,故C错误;
D.t4-t5时间段,逆反应速率大于正反应速率,则化学平衡逆向移动,故D错误;
故选A.
点评 本题考查化学反应速率与化学平衡图象,为高频考点,把握图象中反应速率的变化及大小是解答本题的关键,注意逆反应速率大于正反应速率时平衡逆向移动,题目难度中等.

练习册系列答案
相关题目
16.甲、乙、丙之间具有如图所示的转化关系.则甲不可能是( )


| A. | N2 | B. | H2S | C. | Mg | D. | Na |
17.下列说法不正确的是( )
| A. | 粘有油脂的试管可以用热的纯碱溶液洗涤 | |
| B. | 食醋中含有乙酸,乙酸可由乙醇氧化得到 | |
| C. | 煤的气化、液化只发生物理变化 | |
| D. | 天然气作为化工原料主要用于合成氨和合成甲醇 |
12.(1)下面不是污水处理方法的是A(填字母)A.过滤法 B.混凝法 C.中和法 D.沉淀法天然水中含有细菌,其主要成分是蛋白质,家庭中能杀灭水中细菌的简单方法:①添加合适的消毒剂、②加热或紫外线消毒等;
(2)现有一杯具有永久硬度的水,其中主要含有MgCl2、CaCl2.利用下列试剂中的一部分或全部,设计软化该水的实验方案.可选试剂:①Ca(OH)2溶液;②NaOH溶液;③饱和Na2CO3溶液;④肥皂水.实验方案:(填写下表)
(3)利用海水得到淡水的方法有蒸馏法、电渗析法等.电渗析法是近年来发展起来的一种较好的海水淡化技术,其原理如图所示.
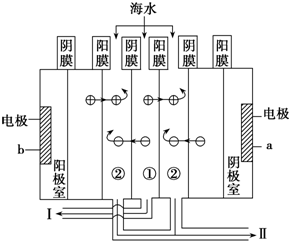
a接电源的负极,Ⅰ口排出的是淡水(填“淡水”或“海水”);
(4)在(3)中某口排出的浓海水中溴元素的质量分数为a%,现用氯气将其中的溴离子氧化为溴单质,则处理1 000t该浓海水需标准状况下的氯气的体积为1400am3.
(2)现有一杯具有永久硬度的水,其中主要含有MgCl2、CaCl2.利用下列试剂中的一部分或全部,设计软化该水的实验方案.可选试剂:①Ca(OH)2溶液;②NaOH溶液;③饱和Na2CO3溶液;④肥皂水.实验方案:(填写下表)
| 实验步骤 |
| 向硬水中加入①(填序数),直到不再产生沉淀为止. |
| 继续向溶液中加入③(填序数),直到不再产生沉淀为止. |
| 将上述混合物过滤(填操作) |

a接电源的负极,Ⅰ口排出的是淡水(填“淡水”或“海水”);
(4)在(3)中某口排出的浓海水中溴元素的质量分数为a%,现用氯气将其中的溴离子氧化为溴单质,则处理1 000t该浓海水需标准状况下的氯气的体积为1400am3.
16.下列实验操作能达到实验目的是( )
| 选项 | 实验操作 | 实验目的 |
| A | 向盛有1mL2%的硝酸银溶液中逐滴加入2%稀氨水,边滴边振荡至最初产生的沉淀恰好消失为止 | 配制少量银氨溶液 |
| B | 向盛有2mL10%的硫酸铜溶液的试管中滴加0.5mL10%氢氧化钠溶液,混合均匀,滴入待检液,加热 | 检验某溶液中是否含有醛基 |
| C | 向淀粉溶液中加入稀硫酸,加热一段时间后,再加入银氨溶液 | 检验淀粉是否水解完全 |
| D | 将氯乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合溶液中滴加硝酸银溶液 | 检验水解产物中的氯离子 |
| A. | A | B. | B | C. | C | D. | D |
17.若NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 在密闭容器中加入3mol H2和1molN2,充分反应后可得到NH3分子数为2NA | |
| B. | 0.1mol/L Na2SO4溶液中含有Na+为0.2NA | |
| C. | 一定条件下,23 g Na与O2反应生成Na2O2时失去的电子数为NA | |
| D. | 标准状况下,22.4L SO3中含有的氯原子数为3NA |
 水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题:
水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题: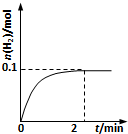 硫-碘循环分解水制氢主要涉及下列反应:
硫-碘循环分解水制氢主要涉及下列反应: