题目内容
已知:2CO(g)+O2(g)=2CO2(g)△H=-566kj/molNa202(s)+CO2(g)=Na2C03(s)+
02(g)△H=-226kj/mol 下列表述正确的是(NA代表阿伏伽德罗常数的数值)( )
| 1 |
| 2 |
| A、lmolCO燃烧时放出的热量为283 kJ/mol |
| B、Na2O2和Na2C03中阴阳离子个数比不同 |
| C、Na202(s)与CO2(g)反应放出226kJ热量时电子转移数为2NA |
| D、Na202(s)+CO(g)=Na2C03(s)△H=-509 kJhnol |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、单位不对;
B、过氧化钠中有钠离子和过氧根离子,2中有钠离子和碳酸根离子;
C、1molNa2O2反应转移1mol电子;
D、利用盖斯定律解答,①÷2+②可得.
B、过氧化钠中有钠离子和过氧根离子,2中有钠离子和碳酸根离子;
C、1molNa2O2反应转移1mol电子;
D、利用盖斯定律解答,①÷2+②可得.
解答:
解:A、1molCO燃烧放热为283KJ,故A错误;
B、1mol过氧化钠中含2mol钠离子和1mol过氧根离子,1mol碳酸钠中含有2mol钠离子和1mol碳酸根离子,Na2O2和Na2CO3中阴阳离子个数比相同,故B错误;
C、1mol过氧化钠与二氧化碳反应放出226KJ的热量同时转移电子数为NA,故C错误;
D、已知:①2CO(g)+O2(g)═2CO2(g)△H=-566kJ?mol-1
②Na2O2(s)+CO2(g)═Na2CO3(s)+
O2(g)△H=-226kJ?mol-1
据盖斯定律,①÷2+②得B,故D正确;
故选:D.
B、1mol过氧化钠中含2mol钠离子和1mol过氧根离子,1mol碳酸钠中含有2mol钠离子和1mol碳酸根离子,Na2O2和Na2CO3中阴阳离子个数比相同,故B错误;
C、1mol过氧化钠与二氧化碳反应放出226KJ的热量同时转移电子数为NA,故C错误;
D、已知:①2CO(g)+O2(g)═2CO2(g)△H=-566kJ?mol-1
②Na2O2(s)+CO2(g)═Na2CO3(s)+
| 1 |
| 2 |
据盖斯定律,①÷2+②得B,故D正确;
故选:D.
点评:本题考查放热多少与燃烧热的单位不同、盖斯定律的应用、过氧化钠在氧化还原反应中转移电子数计算以及过氧化钠中阴阳离子数等等,题目难度中等.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
下列物质中,能跟NaOH溶液反应放氢气的是( )
| A、Mg | B、Al |
| C、S | D、Cl2 |
下列反应过程中的能量变化符合如图情况的是( )
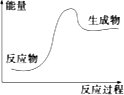

| A、酸与碱的中和反应 |
| B、Ba(OH)2?8H2O与NH4Cl的反应 |
| C、镁和盐酸的反应 |
| D、酒精燃烧 |
雌黄与浓硝酸反应如下:As2S3+28HNO3(浓)?2H3As04+3H2S04+28N02↑+8H2O,下列说法正确的是( )
| A、氧化产物只有H2S04 |
| B、1mol As2S3发生反应,有28 mol电子转移 |
| C、该反应中As2S3既是氧化剂又是还原剂 |
| D、As2S3不可能与氧气反应 |
短周期主族元素A、B、C、D,原子半径依次减小,其中A的单质是一种重要的半导体材料;B的单质常用于自来水消毒;C是金属,其密度是所有金属中最小;D的一种气态氢化物能使湿润的红色石蕊试纸变蓝.则下列说法错误的是( )
| A、D的气态氢化物比A的气态氢化物稳定 |
| B、A的常见氧化物是一种酸性氧化物,能与水反应生成一种弱酸 |
| C、B的最高价氧化物对应的水化物是酸性最强的含氧酸 |
| D、单质C常温下能与水反应生成一种气体 |
生产、生活离不开各种化学物质,下列说法不正确的是( )
| A、不需要通过化学反应就能从海水中获得食盐和淡水 |
| B、潜水艇在紧急情况下可用过氧化钠供氧 |
| C、氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
| D、“加碘盐”、“高钙牛奶”、“补铁营养品”等食品中的碘、钙、铁是指单质 |
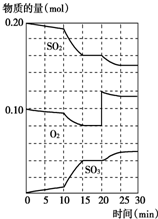 600℃时,在一固定容积的密闭容器中,将二氧化硫和氧气混合发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0.反应过程中SO2、O2、SO3物质的量的变化如图,下列说法错误的是( )
600℃时,在一固定容积的密闭容器中,将二氧化硫和氧气混合发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0.反应过程中SO2、O2、SO3物质的量的变化如图,下列说法错误的是( )| A、反应从开始到第一次平衡时,二氧化硫的转化率为20% |
| B、10~15 min和20~25min相比,前者的化学反应速率大 |
| C、反应进行至20min时,曲线发生变化是因为通入了氧气 |
| D、反应进行到10min~15 min的曲线变化原因一定是增大了压强 |
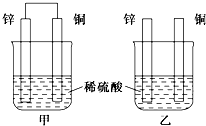 将纯锌片和纯铜片按下图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
将纯锌片和纯铜片按下图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题: