题目内容
4.下列说法错误的是( )| A. | 催化剂可以改变化学反应速率 | |
| B. | 食物放在冰箱中会减慢食物变质的速率 | |
| C. | 2molSO2与 1molO2一定能生成2molSO3 | |
| D. | 锌与稀硫酸反应时,加入少量铜粉能加快反应 |
分析 A.催化剂可改变活化分子百分数;
B.温度降低,反应速率减小;
C.反应为可逆反应;
D.可形成原电池反应.
解答 解:A.催化剂可改变活化分子百分数,可改变反应速率,故A正确;
B.温度降低,活化分子百分数减小,反应速率减小,故B正确;
C.反应为可逆反应,转化率不可能达到100%,故C错误;
D.锌置换出铜,可形成原电池反应而加快反应速率,故D正确.
故选C.
点评 本题考查反应速率的因素,为高频考点,把握影响反应速率的常见因素为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.下列装置或操作能达到实验目的是( )
| A. |  分离乙酸和乙醇 | B. |  构成锌铜原电池 | C. | 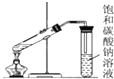 制备乙酸乙酯 | D. | 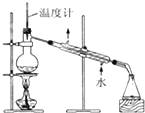 制备蒸馏水 制备蒸馏水 |
15.下列说法正确的是( )
| A. | 科学家在宇宙深处发现了H3+与H3,二者互为同位素 | |
| B. | 焰色反应实验操作过程中,没有铂丝,也可以用光洁无锈的铁丝代替 | |
| C. | N2的结构式为N≡N,电子式为 | |
| D. | Na+的结构示意图  |
12.下列关于钠的氧化物的说法正确的是( )
| A. | Na2O2是白色固体,与冷水作用放出氧气,生成氢氧化钠 | |
| B. | 在Na2O2与CO2的反应中,氧化剂是Na2O2,还原剂是CO2 | |
| C. | Na2O不稳定,能继续被氧化,生成Na2O2 | |
| D. | Na2O2能与水反应,生成NaOH,所以Na2O2是碱性氧化物 |
19.石油和煤都是重要的化石能源,下列有关石油和煤的叙述正确的是( )
| A. | 都是纯净物 | B. | 都含有碳元素 | C. | 都是可再生能源 | D. | 都属于单质 |
13.在容积不变的密闭容器中,可逆反应H2(g)+I2(g)?2HI(g)达到平衡的标志( )
| A. | H2、I2、HI的浓度之比1:1:2 | |
| B. | H2、I2、HI的浓度保持不变 | |
| C. | 混合气体的密度保持不变 | |
| D. | 容器内气体的总压强不随时间变化而变化 |
14.环烷烃是一类饱和烃,下面依次是环丙烷、环丁烷、环戊烷及环丙烷的一种衍生物的化学性质下列说法正确的是( )
①△+Br2→BrCH2CH2CH2Br
②□+Br2→BrCH2CH2CH2CH2Br
③ +Br2→BrCH2CH2CH2CH2CH2Br
+Br2→BrCH2CH2CH2CH2CH2Br
④
①△+Br2→BrCH2CH2CH2Br
②□+Br2→BrCH2CH2CH2CH2Br
③
 +Br2→BrCH2CH2CH2CH2CH2Br
+Br2→BrCH2CH2CH2CH2CH2Br④

| A. | 环烷烃与烷烃都是饱和烃,所以具有相同的通式 | |
| B. | B所有的饱和烃都不能发生加成反应 | |
| C. | 可用溴水鉴别丙烯与环丙烷 | |
| D. | 可用酸性高锰酸钾溶液鉴别丙烯与环丙烷 |
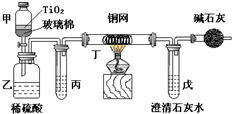 电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.