题目内容
3.工业上电解制碱的技术是用离子交换膜法,主要原料是饱和食盐水.请回答下列问题:(1)阳离子交换膜把电解槽隔成了阴极室和阳极室,电解食盐水时,它只允许H+和Na+ (填离子符号)通过.
(2)为了去除粗盐中混有的Ca2+、Mg2+、SO42-,下列选项中所加试剂(均为溶液)及加入顺序均合理的是B (填选项字母)
A.先加足量的BaCl2,再加足量的Na2CO3,最后加入适量稀盐酸
B.先加入足量的NaOH,再加入足量的BaCl2,然后加入足量Na2CO3,最后加入适量稀盐酸
C.先加足量的Na2CO3,再加足量的BaCl2,然后加足量的NaOH,最后加入适量稀盐酸
D.先加足量的Ba(NO3)2,再加足量NaOH,然后再加足量的Na2CO3,最后加入适量稀盐酸
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节电能30%以上.在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子交换膜都只允许阳离子通过.
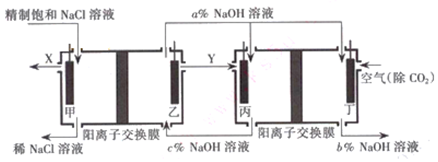
①图中X是氯气 (填化学式),分析比较图示中a、b、c从大到小的顺序为c>a>b.
②写出燃料电池中负极上发生的电极反应式2H2+4OH--4e-=4H2O.
③这样设计的主要节电能之处在于(任写出一条)燃料电池可以补充电解池消耗的电能、提高产出碱液的浓度.
分析 (1)阳离子交换膜只允许阳离子通过,而阴离子不能通过;
(2)除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠,要先加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除过量的钡离子;
(3)①由于在燃料电池中氧气在正极放电,可燃性气体在负极放电,所以通入空气的极是正极,则通入可燃性气体Y的极是负极,根据在氯碱工业中,电解食盐水除了生成NaOH还生成氯气和氢气,和空气形成燃料电池的为氢气,即Y是氢气,则X是氯气;
燃料电池中的离子膜只允许阳离子通过,而燃料电池中正极氧气得到电子产生OH-,所以反应后氢氧化钠的浓度升高,即a%小于c%,可知NaOH浓度增大;
②燃料电池中负极氢气失电子发生氧化反应;
③根据燃料电池能将化学能转化为电能结合该方法来分析其优点之处.
解答 解:(1)阳离子交换膜只允许阳离子H+和Na+通过,而阴离子氢氧根和氯离子均不能通过,故答案为:H+和Na+;
(2)要先除硫酸根离子,然后再除钙离子,碳酸钠可以除去过量的钡离子,如果加反了,过量的钡离子就没法除去,至于加氢氧化钠除去镁离子顺序不受限制,因为过量的氢氧化钠加盐酸就可以调节了,只要将三种离子除完了,过滤就行了,最后加盐酸除去过量的氢氧根离子碳酸根离子,故选:B;
(3)①由于在燃料电池中氧气在正极放电,可燃性气体在负极放电,所以通入空气的极是正极,则通入可燃性气体Y的极是负极,根据在氯碱工业中,电解食盐水除了生成NaOH还生成氯气和氢气,和空气形成燃料电池的为氢气,即Y是氢气,则X是氯气;
燃料电池中的离子膜只允许阳离子通过,而燃料电池中正极氧气得到电子产生OH-,所以反应后氢氧化钠的浓度升高,即a%大于b%,负极氢气失电子生成氢离子消耗氢氧根离子,所以c%>a%,得到c%>a%>b%,故答案为:c>a>b,
故答案为:氯气;c>a>b;
②燃料电池中负极氢气失电子发生氧化反应,电极反应式为2H2+4OH--4e-=4H2O,故答案为:2H2+4OH--4e-=4H2O;
③据装置特点及反应过程可知,这样设计的优点是燃料电池可以补充电解池消耗的电能;提高产出碱液的浓度;降低能耗等,
故答案为:燃料电池可以补充电解池消耗的电能、提高产出碱液的浓度.
点评 本题考查了电解原理,为高频考点,侧重于学生的分析能力和计算能力的考查,明确离子交换膜的作用及阴阳极上发生的反应是解本题关键,题目难度中等.

(1)常温下,有pH相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
①加水稀释10倍后,醋酸溶液中的c(H+)>盐酸溶液中的c(H+)(填“>”、“=”或“<”).
②加等浓度的NaOH溶液至恰好恰好中和,所需NaOH溶液的体积:醋酸>盐酸(填“>”、“=”或“<”).
③使温度都升高20℃,溶液中c(H+):醋酸>盐酸(填“>”、“=”或“<”).
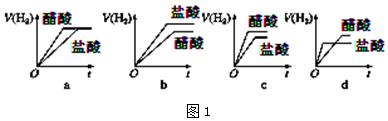
④分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图(图1)正确的是
c(填字母).
(2)图2是不的电解质溶液中加入新物质时溶液的导电性能发生变化性情况(电流强度(I)随新物质加入量(m)的变化曲线),将对应的图象字母填写在下列横线上.
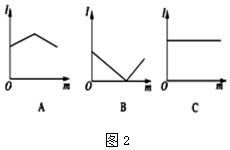
①氢氧化钡溶液中滴入硫酸溶液至过量B.
②醋酸溶液中滴入氨水至过量A.
③澄清石灰水中通入CO2至过量B.
(3)已知表中的电离平衡常数,回答问题
| K1 | K2 | |
| H2SO3 | 1.54×10-2 | 1.02×10-7 |
| H2CO3 | 4.3×10-7 | 5.6×10-11 |
②H2SO3溶液与NaHCO3溶液反应的主要离子方程式为H2SO3+HCO3-=HSO3-+CO2↑+H2O.
| A. | Na>O | B. | Na+>O2- | C. | Mg>Na | D. | Mg2+>Na+ |
| A. | 氧化剂 | B. | 还原剂 | C. | 溶剂 | D. | 催化剂 |
| A. | 氨气通入醋酸溶液CH3COOH+NH3═CH3COONH4 | |
| B. | 澄清的石灰水跟盐酸反应H++OH-═H2O | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+═Cu2++Ag | |
| D. | 碳酸钙跟盐酸反应CaCO3+2HCl═2Ca++H2CO3↑ |
| A. | 二氧化硫可广泛用于食品的增白 | |
| B. | 用硫酸清洗锅垢中的水垢 | |
| C. | 用SO2漂白纸浆和草帽辫 | |
| D. | 因为浓硫酸有强氧化性,故浓硫酸可用于干燥H2和CO |