题目内容
13.高铁酸钾(K2FeO4,暗紫色固体),是一种新型、高效、多功能的水处理剂,完成下列填空:(1)K2FeO4溶于水得到浅紫红色的溶液,且易水解,生成氧气和氢氧化铁.写出该水解反应的离子方程式4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2;说明高铁酸钾做水处理剂的原理高铁酸根离子具有强氧化性,能杀菌消毒,氢氧化铁吸附水中的悬浮物.
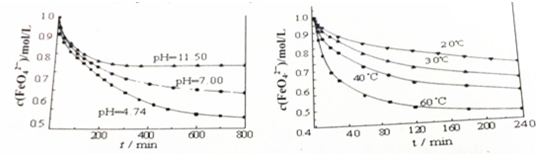
(2)如图分别是1mol/L的K2FeO4溶液在不同pH和温度下c(FeO42-)随时间的变化曲线.
根据以上两图,说明配置K2FeO4溶液的注意事项低温、碱性条件下配制溶液.
(3)钢铁厂的副产品SO2多用于制硫酸和石膏等
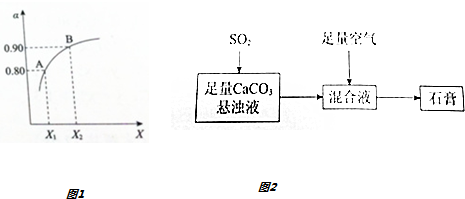
①制硫酸最重要的反应是:2SO2(g)+O2(g)?2SO3(g)+196kJ如图1表示将2.0molSO2和一定量的O2置于1L密闭容器中,当其他条件一定时,SO2(g)的平衡转化率α随X的变化关系,则X(X1、X2)可以代表的物理量是压强或氧气的量.
②如图2表示生产石膏的简单流程,请用平衡移动原理解释向CaCO3悬浊液中通入SO2发生反应的原因SO2与水会反应:SO2+H2O?H2SO3;生成的H2SO3会部分电离:H2SO3?H++HSO3-;CaCO3悬浊液中存在CaCO3?Ca2+(aq)+CO32-(aq),向CaCO3悬浊液中通入SO2时,CO32-与H+反应,c(CO32-)减小,溶解平衡正向移动..
分析 (1)用K2FeO4处理中性废水时与水反应生成氢氧化铁胶体,并放出无色无味的气体和其它物质,铁元素化合价降低,氧元素化合价升高生成氧气,结合电荷守恒配平书写离子方程式;氢氧化铁胶体具有吸附作用;
(2)依据图中数据结合高铁酸根离子水解反应的特点判断解答;
(3)①2SO2(g)+O2(g)?2SO3(g),为可逆反应,正向为气体体积减小的反应,依据浓度、压强对化学平衡移动影响解答;
②碳酸钙的悬浊液中存在溶解平衡,所以而通入二氧化硫与水反应生成亚硫酸酸性比碳酸的酸性强;
解答 解:(1)用K2FeO4处理中性废水时与水反应生成氢氧化铁胶体,并放出无色无味的气体和其它物质,铁元素化合价降低,氧元素化合价升高生成氧气,结合电荷守恒配平书写离子方程式为:4FeO42-+10H2O=4Fe(OH)3(胶体)+8OH-+3O2↑;高铁酸根离子具有强氧化性,能杀菌消毒,氢氧化铁吸附水中的悬浮物;
故答案为:4FeO42-+10H2O=4Fe(OH)3(胶体)+8OH-+3O2↑;
高铁酸根离子具有强氧化性,能杀菌消毒,氢氧化铁吸附水中的悬浮物;
(2)高铁酸根离子水解方程式:4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2,依据图中数据可知升高温度,减小pH值,高铁酸根离子浓度降低,所以应在低温、碱性条件下配制高铁酸钾溶液;
故答案为:低温、碱性条件下配制溶液;
(3)①依据图中数据可知,随着X量加入SO2(g)的平衡转化率α逐渐增大,反应2SO2(g)+O2(g)?2SO3(g),为气体体积减小的反应,加压平衡向正向移动;多种反应物的,增大一种反应物浓度可以提高其他反应物转化率,所以对反应2SO2(g)+O2(g)?2SO3(g),增大氧气的用量能够提高二氧化硫转化率,图中X可以是压强或氧气的量;
故答案为:压强或氧气的量;
②CaCO3悬浊液中存在CaCO3?Ca2+(aq)+CO32-(aq),向CaCO3悬浊液中通入SO2时,SO2与水会反应:SO2+H2O?H2SO3;生成的H2SO3会部分电离:H2SO3?H++HSO3-,CO32-与H+反应,c(CO32-)减小,溶解平衡正向移动;
故答案为:SO2与水会反应:SO2+H2O?H2SO3;生成的H2SO3会部分电离:H2SO3?H++HSO3-;CaCO3悬浊液中存在CaCO3?Ca2+(aq)+CO32-(aq),向CaCO3悬浊液中通入SO2时,CO32-与H+反应,c(CO32-)减小,溶解平衡正向移动.
点评 本题为综合题,考查了不同价态铁之间的转化,化学平衡移动原理及其应用,明确高铁酸根离子的性质、熟悉影响化学平衡移动的因素是解题关键,题目难度中等.

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案| A. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| B. | 0.5mol/L亚硫酸钠溶液中含有的SO32-的物质的量为0.5mol | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 过量铜片与100mL18mol/L的浓硫酸反应,转移的电子数为1.8NA |
| A. | Na+、Fe3+是人体所需微量元素 | B. | 苯酚不能用于杀菌消毒 | ||
| C. | 氢气是未来的一种理想燃料 | D. | 乙醇是不可再生的生物质能源 |
 +12MnO${\;}_{4}^{-}$+36H+→
+12MnO${\;}_{4}^{-}$+36H+→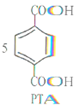 +12Mn2++28H2O.
+12Mn2++28H2O.| A. | PTA是该反应的氧化产物 | B. | 消耗1molPX,共转移8mol电子 | ||
| C. | PX含苯环的同分异构体还有3种 | D. | PTA与乙二醇可以发生缩聚反应 |
| 物质(少量杂质) | 操作 | |
| A | KNO3固体(NaCl) | 加水溶解、蒸发结晶、趁热过滤、洗涤、干燥 |
| B | NaCl固体(KNO3) | 加水溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
| C | FeCl3溶液(NH4Cl) | 加热蒸干、灼烧 |
| D | NH4Cl溶液(FeCl3) | 滴加氨水至不再产生沉淀为止,过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 氧化性酸:HNO3、H3PO4、HClO4 | |
| B. | 干燥剂:碱石灰、硅胶、无水氯化钙 | |
| C. | 酸性氧化物:SiO2、Cl2O、CrO3 | |
| D. | 危险化学品:天然气、金属钠、氯酸钾 |
| A. | 沸点由低到高的顺序为:CH3CH2CH3<CH3(CH2)2CH3<(CH3)3CH | |
| B. | 工业上合成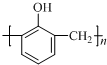 的单体为甲醛和苯酚( 的单体为甲醛和苯酚(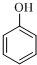 ) ) | |
| C. | 相同质量的乙烯和乙酸完全燃烧时,消耗氧气的量相同 | |
| D. | 某烷烃可以命名为2,3,3-三甲基-4-乙基戊烷 |
| A. | 该电池的工作环境应在高温条件下 | |
| B. | 正极反应:O2+2H2O+4e-═4OH- | |
| C. | 电池工作时葡萄糖在负极上失去电子发生还原反应 | |
| D. | 电池工作时H+由负极移向正极,电解质溶液的pH增大 |
| t/s | 0 | 500 | 1000 |
| C(H2O)/mol•L-1 | 5.00 | 3.52 | 2.48 |
| C(CO2)/mol•L-1 | 2.50 |
| A. | 在500s内用H2O(g)表示的化学反应速率是2.96×10-3mol•L-1•s-1 | |
| B. | 在500s时生成的CH4的浓度是0.74mol•L-1 | |
| C. | 在1000s时反应达到平衡 | |
| D. | 0-500s的平均反应速率大于500~1000s的平均反应速率 |