题目内容
13.甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和水,已知室温下1g甲硅烷自燃放出热量44.6kJ,其热化学方程式,甲硅烷(SiH4)的燃烧热为1427.2kJ•mol-1.分析 根据甲硅烷的质量计算1mol甲硅烷燃烧放出的热量,结合化学方程式书写热化学方程式.注意物质的聚集状态和反应热的单位等问题;
解答 解:n(SiH4)=$\frac{1g}{32g/mol}$=$\frac{1}{32}$mol,则1molSiH4燃烧放出的热量为:44.6kJ×32=1427.2kJ,
反应的化学方程式为:SiH4+O2=SiO2+H2O,则热化学方程式为:SiH4(g)+O2(g)=SiO2(g)+2H2O;△H=-1427.2kJ/mol,
故答案为:1427.2.
点评 本题考查热化学方程式的书写,题目难度不大,注意热化学方程式的书写方法应用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.某研究小组利用“钯催化交叉偶联反应”合成了有机物丙,合成路线如下:
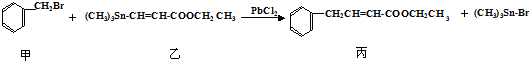
下列分析判断正确的是( )

下列分析判断正确的是( )
| A. | 分离提纯有机物丙宜在NaOH热溶液中进行 | |
| B. | PbCl2的作用是提高反应物的活性,加快反应速率 | |
| C. | 可用酸性KMnO4溶液检验有机物丙中是否含有机物乙 | |
| D. | 利用NaOH溶液、AgNO3溶液即可确定有机物甲中含有溴元素 |
8.已知:4NH3(g)+5O2(g)?4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列关系不正确的是( )
| A. | 4v(NH3)=5v(O2) | B. | 6v(O2)=5v(H2O) | C. | 3v(NH3)=2v(H2O) | D. | 4v(O2)=5v(NO) |
18.下列关于各反应类型的关系中,说法正确的是( )
| A. | 没有单质参加的化合反应一定不属于氧化还原反应 | |
| B. | 离子反应一定属于氧化还原反应 | |
| C. | 有的复分解反应属于氧化还原反应 | |
| D. | 置换反应一定属于氧化还原反应 |
5.下列反应的离子方程式书写不正确的是( )
| A. | 实验室制取氯气 MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| B. | 过量的氨水滴加到氯化铝溶液中 Al3++3NH3.H2O═Al(OH)3↓+3NH4+ | |
| C. | 氯气与水反应:Cl2+H2O═Cl-+H++HClO | |
| D. | 小苏打溶液中加入过量石灰水2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
2.下列说法正确的是( )
| A. | 在101 kPa时,1 mol H2完全燃烧生成气态水,放出285.8 kJ热量,H2的燃烧热为-285.8 kJ•mol-1 | |
| B. | 测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度,NaOH起始温度和反应后终止温度 | |
| C. | 在101 kPa时,1 mol C与适量O2反应生成1 mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ•mol-1 | |
| D. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.31 kJ•mol-1.若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ |
3. 向FeCl3、CuCl2混合溶液中通入H2S和O2的混合气体可回收S,其转化关系如图.相关说法不正确的是( )
向FeCl3、CuCl2混合溶液中通入H2S和O2的混合气体可回收S,其转化关系如图.相关说法不正确的是( )
 向FeCl3、CuCl2混合溶液中通入H2S和O2的混合气体可回收S,其转化关系如图.相关说法不正确的是( )
向FeCl3、CuCl2混合溶液中通入H2S和O2的混合气体可回收S,其转化关系如图.相关说法不正确的是( )| A. | 反应I的基本反应类型是复分解反应 | |
| B. | 反应II中每生成1molS需要2molFeCl3 | |
| C. | 在转化过程中能循环利用的物质有FeCl2和CuCl2 | |
| D. | 在转化过程中化合价不变的元素只有Cu和Cl |