题目内容
用0.20mol/L盐酸滴定未知浓度的氢氧化钠溶液,根据实验回答下列有关问题.
(1)带有玻璃活塞的滴定管盛放 ;用酚酞作指示剂,滴定到达终点时,溶液的颜色变化是
(2)根据下表的数据,计算待测氢氧化钠溶液的物质的量浓度是 .
(3)实验过程中存在着下列操作,请将其对测定结果产生的影响填在空格中(填“偏高”、“偏低”或“无影响”).
①盛盐酸的滴定管在装酸液前未用盐酸润洗,则滴定结果 .
②开始时滴定管尖嘴处有气泡,在滴定过程中气泡消失,则滴定结果 .
③锥形瓶未用待测的NaOH溶液润洗,则滴定结果 .
④开始平视读数,滴定结束后俯视读数,则滴定结果 .
(1)带有玻璃活塞的滴定管盛放
(2)根据下表的数据,计算待测氢氧化钠溶液的物质的量浓度是
| 滴定次数 | 待测液体积(mL) | 标准酸液的体积 | |
| 滴定前刻度(mL) | 滴定后刻度(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
①盛盐酸的滴定管在装酸液前未用盐酸润洗,则滴定结果
②开始时滴定管尖嘴处有气泡,在滴定过程中气泡消失,则滴定结果
③锥形瓶未用待测的NaOH溶液润洗,则滴定结果
④开始平视读数,滴定结束后俯视读数,则滴定结果
考点:中和滴定
专题:实验题
分析:(1)带有玻璃活塞的滴定管为酸式滴定管,根据酸性溶液盛放在酸式滴定管中;锥形瓶中溶液的颜色由浅红变无色且保持30秒内不褪色;
(2)先判断数据的合理性,然后盐酸的平均体积,然后根据HCl~NaOH求氢氧化钠的物质的量浓度;
(3)根据c(待)=
判断不当操作对相关物理量的影响;
(2)先判断数据的合理性,然后盐酸的平均体积,然后根据HCl~NaOH求氢氧化钠的物质的量浓度;
(3)根据c(待)=
| c(标)×V(标) |
| V(待) |
解答:
解:(1)带有玻璃活塞的滴定管为酸式滴定管,用来盛放0.20mol/L盐酸;滴定时,锥形瓶中溶液的颜色由浅红变无色且保持30秒内不褪色,可说明达到滴定终点;
故答案为:0.20mol/L盐酸;锥形瓶中溶液的颜色由浅红变无色且保持30秒内不褪色.
(2)两次消耗的盐酸的体积为19.90mL,20.10mL,均有效,盐酸溶液的平均体积为20.00mL
HCl~NaOH
1 1
0.20mol/L×20.00mL C×10.00mL
解得:C(NaOH)=0.40mol/L
故答案为:0.40mol/L;
(3)①盛盐酸的滴定管在装酸液前未用盐酸润洗,标准液浓度降低,造成V(标)偏大,根据c(待)=
判断,可知c(待)偏高;
②开始时滴定管尖嘴处有气泡,在滴定过程中气泡消失,造成V(标)偏大,根据c(待)=
判断,可知c(待)偏高;
③锥形瓶未用待测的NaOH溶液润洗,待测液的物质的量不变,对V(标)无影响,根据c(待)=
判断,可知c(待)无影响;
④开始平视读数,滴定结束后俯视读数,造成V(标)偏小,根据c(待)=
判断,可知c(待)偏低;
故答案为:①偏高 ②偏高 ③无影响 ④偏低;
故答案为:0.20mol/L盐酸;锥形瓶中溶液的颜色由浅红变无色且保持30秒内不褪色.
(2)两次消耗的盐酸的体积为19.90mL,20.10mL,均有效,盐酸溶液的平均体积为20.00mL
HCl~NaOH
1 1
0.20mol/L×20.00mL C×10.00mL
解得:C(NaOH)=0.40mol/L
故答案为:0.40mol/L;
(3)①盛盐酸的滴定管在装酸液前未用盐酸润洗,标准液浓度降低,造成V(标)偏大,根据c(待)=
| c(标)×V(标) |
| V(待) |
②开始时滴定管尖嘴处有气泡,在滴定过程中气泡消失,造成V(标)偏大,根据c(待)=
| c(标)×V(标) |
| V(待) |
③锥形瓶未用待测的NaOH溶液润洗,待测液的物质的量不变,对V(标)无影响,根据c(待)=
| c(标)×V(标) |
| V(待) |
④开始平视读数,滴定结束后俯视读数,造成V(标)偏小,根据c(待)=
| c(标)×V(标) |
| V(待) |
故答案为:①偏高 ②偏高 ③无影响 ④偏低;
点评:本题主要考查酸碱滴定实验的基本操作,学生应注意操作的规范性和实验中常见的误差分析.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
阿伏加德罗常数用NA表示,下列叙述正确的是( )
| A、常温常压下,1 mol NO2中含有的分子数为 NA |
| B、常温常压下,0.2mol铁在0.2 mol氯气中充分燃烧,转移的电子数为 0.6NA |
| C、7.8g过氧化钠粉末与足量二氧化硫反应转移的电子数为0.2NA |
| D、11.2L Cl2通入足量氢氧化钠溶液中充分反应,转移的电子数为0.5NA |


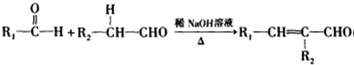 (R1、R2为烃基或氢原子);
(R1、R2为烃基或氢原子); (R1、R2为烃基)
(R1、R2为烃基)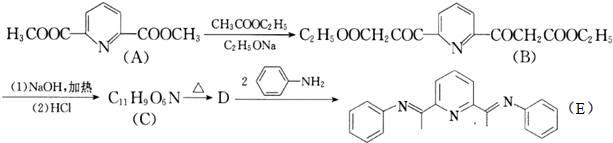
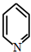 )且环上只有2个取代基;
)且环上只有2个取代基;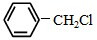 和
和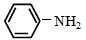 为原料合成西佛碱N-苯基苯甲亚胺(
为原料合成西佛碱N-苯基苯甲亚胺(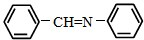 ),请你拟出合成路线:
),请你拟出合成路线:
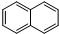 )的衍生物;
)的衍生物;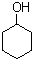 为原料制备化合物B的合成路线流程图(无机试剂任选).合成路线流程图示例如下:H2C═CH2
为原料制备化合物B的合成路线流程图(无机试剂任选).合成路线流程图示例如下:H2C═CH2