题目内容
1. 甲醇(CH3OH)是一种重要的化工原料,也是一种比较理想的燃料.甲醇在各个领域有着广泛的应用.
甲醇(CH3OH)是一种重要的化工原料,也是一种比较理想的燃料.甲醇在各个领域有着广泛的应用.(1)已知:①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H1=-1275.6kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H2=-566.0kJ•mol-1
③H2O(g)═H2O(l)△H3=-44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-266.8kJ•mol-1 .
(2)燃料电池是一种连续地将燃料和氧化剂的化学能直接转换成电能的化学电池.如图是一个化学过程的示意图:
2CH3OH+3O2+4KOH$?_{充电}^{放电}$ K2CO3+6H2O
①A(石墨)电极的名称是阳极
②通入O2的电极的电极反应式是O2+2H2O+4e-=4OH-
③乙池中反应的化学方程式为4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+O2↑+4HNO3
④当电路中通过0.01mol电子时,丙池溶液的pH=1(忽略电解过程中溶液体积的变化).
(3)合成甲醇的主要反应是:2H2(g)+CO(g)?CH3OH(g)△H=-90.8kJ•mol-1.
①在恒温恒容条件下,充入一定量的H2和CO,发生反应2H2(g)+CO(g)?CH3OH(g).则该反应达到平衡状态的标志有bcd
a.混合气体的密度保持不变 b.混合气体的总压强保持不变
c.CO的质量分数保持不变 d.甲醇的浓度保持不变
e.v正(H2)=v逆(CH3OH) f.v(CO)=v(CH3OH)
②要提高反应2H2(g)+CO(g)?CH3OH(g)中CO的转化率,可以采取的措施是:df
a.升温 b.加入催化剂c.增加CO的浓度d.加入H2 e.加入惰性气体 f.分离出甲醇
(4)生产甲醇的原料CO和H2来源于:CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0一定条件下CH4的平衡转化率与温度、压强的关系如图a.则T1<T2(填“<”“>”或“=”).

分析 (1)根据盖斯定律,将已知反应(①-②-③×4)÷2得到CH3OH(l)+O2(g)=CO(g)+2H2O(l),焓变进行相应的改变;
(2)甲池能自发的进行氧化还原反应,属于原电池,通入甲醇的电极为负极、通入氧气的电极为正极,则乙池、丙池是电解池,A、C属于阳极,B、D属于阴极,A电极反应式为氢氧根离子得电子生成氧气,B极反应式为Ag++e-=Ag、C极反应式为4OH-+4e-=2H2O+O2↑、D极反应式为Cu2++2e-=Cu;
(3)①平衡状态时正逆反应速率相等,各组分的浓度保持不变;
②要提高CO的转化率,应使平衡向正反应方向移动;
(4)正反应为吸热反应,压强一定时,升高温度,平衡向正反应方向移动,甲烷的转化率增大,据此判断温度大小.
解答 解:(1)根据盖斯定律,将已知反应(①-②-③×4)÷2得到CH3OH(l)+O2(g)=CO(g)+2H2O(l),所以该反应的△H=$\frac{1}{2}$[(-1275.6kJ/mol)-(-566.0kJ/mol)-(-44.0kJ/mol)×4]=-266.8kJ•mol-1,即CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-266.8kJ•mol-1,
故答案为:CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-266.8kJ•mol-1 ;
(2)①甲池能自发的进行氧化还原反应,属于燃料电池,为原电池,通入甲醇的电极为负极、通入氧气的电极为正极,乙为电解池,A连接原电池正极,则为阳极,
故答案为:阳极;
②碱性条件下,氧气得电子生成氢氧根离子,电极反应式为O2+2H2O+4e-=4OH-,
故答案为:O2+2H2O+4e-=4OH-;
③乙池为电解硝酸银溶液的电解池,生成Ag和氧气,电解方程式为4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+O2↑+4HNO3,
故答案为:4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+O2↑+4HNO3;
④丙池中C极反应式为4OH-+4e-=2H2O+O2↑、D极反应式为Cu2++2e-=Cu,当电路中通过0.01mol电子时,有0.01mol氢氧根离子反应,生成0.01mol氢离子,所以c(H+)=$\frac{0.01mol}{0.1L}$=0.1mol/L,溶液的pH=1,故答案为:1;
(3)①a.容器体积不变,混合气体的质量不变,所以密度始终不变,混合气体的密度保持不变不能说明反应达到平衡状态,故a错误;
b.该反应前后气体物质的量不同,恒容容器中混合气体的总压强保持不变,说明各组分浓度不变,反应达到平衡状态,故b正确;
c.CO的质量分数保持不变,说明反应达到平衡状态,故c正确;
d.甲醇的浓度保持不变,说明反应达到平衡状态,故d正确;
e.氢气以甲醇的化学计量数不同,v正(H2)=v逆(CH3OH),不能说明正逆反应速率相等,不能说明反应达到平衡状态,故e错误;
f.v(CO)=v(CH3OH),无法判断正逆反应速率相等,故f错误;
故答案为:bcd;
②要提高CO的转化率,应使平衡向正反应方向移动,
a.该反应放热,升温平衡逆向移动,故错误;
b.加入催化剂不影响平衡移动,故错误;
c.增加CO的浓度,CO的转化率降低,故错误;
d.加入H2平衡正向移动,CO的转化率增大,故正确;
e.体积不变加入惰性气体,平衡不移动,故错误;
f.分离出甲醇平衡正向移动,CO的转化率增大,故正确;
故答案为:df;
(4)由图开始,压强一定时,温度T2的转化率较大,正反应为吸热反应,升高温度,平衡向正反应方向移动,甲烷的转化率增大,故温度Tl<T2,故答案为:<.
点评 本题考查较综合,涉及化学平衡影响因素、化学平衡状态判断、盖斯定律、原电池和电解池原理等知识点,侧重考查学生分析判断及知识综合应用能力,会正确书写电极反应式,注意:只有反应前后改变的物理量才能作为化学平衡状态判断依据,题目难度不大.

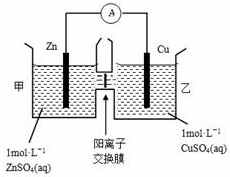
| A. | 铜电极上发生氧化反应 | |
| B. | 电池工作一段时间后,乙池溶液的总质量增加 | |
| C. | 电池工作一段时间后,乙池的c(Zn2+)>c(SO42-) | |
| D. | 阴、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡 |
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |

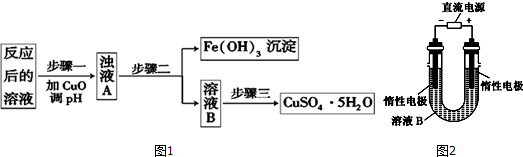
| A. | 当m2-m3=2.96 g时,Fe3O4的质量至少为2.32g | |
| B. | 生成蓝色溶液的离子方程式为Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 要确定混合物中是否含有Al,可取A加入适量稀盐酸 | |
| D. | 当m1>m2时,溶液a中的阴离子只有1种 |
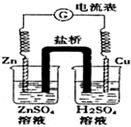
| A. | 随着反应进行,左烧杯中盐溶液浓度上升,右烧杯中酸溶液浓度下降 | |
| B. | 盐桥的作用是让电子通过,以构成闭合回路 | |
| C. | 随着反应进行,右烧杯中溶液pH变小 | |
| D. | 总反应为:2H++Zn═H2↑+Zn2+ |
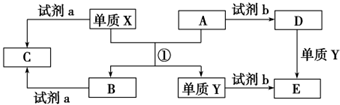

 A、B、C、D、E、F六种元素为前四周期元素,原子序数依次增大.A的最高正价和最低负价的绝对值相等,B的基态原子的电子分布在3个不同的能级且各能级中电子数相等.D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子的s能级的电子总数与p能级的电子数相等,F的基态原子在同周期元素中未成对电子数最多.请回答下列问题:
A、B、C、D、E、F六种元素为前四周期元素,原子序数依次增大.A的最高正价和最低负价的绝对值相等,B的基态原子的电子分布在3个不同的能级且各能级中电子数相等.D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子的s能级的电子总数与p能级的电子数相等,F的基态原子在同周期元素中未成对电子数最多.请回答下列问题: ;
;