题目内容
无水AlCl3易升华,可用作有机合成的催化剂等.工业上用铝土矿(Al2O3、Fe2O3)为原料制备无水AlCl3的工艺流程如图:
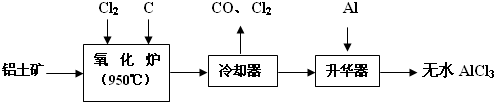
(1)氧化炉中Al2O3、Cl2和C反应的化学方程式 .
(2)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,此反应的离子方程式 .
(3)为了测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,再洗涤、灼烧、冷却、称重、计算.试写出样品溶于过量NaOH溶液过程中有关反应的离子方程式:
(4)工业上另一种由铝灰为原料制备无水AlCl3工艺中,最后一步是由AlCl3?6H2O脱去结晶水制备无水AlCl3,实验这一步操作方法是在 (填试剂)气流中加热.
(5)工业上铝土矿经提纯后可冶炼铝,在950-970℃和冰晶石作用下进行电解,若电解过程中制得2.7吨铝,理论上转移电子的数目为 NA (Al:27)

(1)氧化炉中Al2O3、Cl2和C反应的化学方程式
(2)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,此反应的离子方程式
(3)为了测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,再洗涤、灼烧、冷却、称重、计算.试写出样品溶于过量NaOH溶液过程中有关反应的离子方程式:
(4)工业上另一种由铝灰为原料制备无水AlCl3工艺中,最后一步是由AlCl3?6H2O脱去结晶水制备无水AlCl3,实验这一步操作方法是在
(5)工业上铝土矿经提纯后可冶炼铝,在950-970℃和冰晶石作用下进行电解,若电解过程中制得2.7吨铝,理论上转移电子的数目为
考点:物质分离和提纯的方法和基本操作综合应用,制备实验方案的设计
专题:实验设计题
分析:(1)根据工艺流程可知升华器中含有AlCl3等,所以Al2O3、C12和C反应会生成A1C13,由冷凝器尾气可知还会生成CO;
(2)Cl2有强氧化性,将SO32-氧化为SO42-,自身被还原为2C1-;
(3)无水AlCl3产品(含杂质FeCl3),溶于过量NaOH溶液过程中,铁离子与氢氧根离子结合成氢氧化铁沉淀,铝离子与氢氧根离子结合成偏铝酸根和水;
(4)AlCl3是强酸弱碱盐,结晶过程中会发生水解,为了防止其发生水解,可在HCl气流中加热脱结晶水;
(5)2Al2O 3
4Al+3O2,转移电子的物质的量等于生成铝的物质的量的3倍.
(2)Cl2有强氧化性,将SO32-氧化为SO42-,自身被还原为2C1-;
(3)无水AlCl3产品(含杂质FeCl3),溶于过量NaOH溶液过程中,铁离子与氢氧根离子结合成氢氧化铁沉淀,铝离子与氢氧根离子结合成偏铝酸根和水;
(4)AlCl3是强酸弱碱盐,结晶过程中会发生水解,为了防止其发生水解,可在HCl气流中加热脱结晶水;
(5)2Al2O 3
| ||
| 电解,冰晶石 |
解答:
解:(1)根据工艺流程可知氯化炉的产物,经冷却、升华可制备无水AlCl3,说明氯化炉的产物中含有A1C13,冷凝器尾气含有CO,所以Al2O3、C12和C反应,生成A1C13和CO,反应方程式为A12O3+3C12+3C
2A1C13+3CO,
故答案为:A12O3+3C12+3C
2A1C13+3CO;
(2)Cl2有强氧化性,将SO32-氧化为SO42-,自身被还原为2C1-.反应离子方程式为SO32-+C12+H2O═SO42-+2C1-+2H+,
故答案为:SO32-+C12+H2O═SO42-+2C1-+2H+;
(3)无水AlCl3产品(含杂质FeCl3),溶于过量NaOH溶液过程中,铁离子与氢氧根离子结合成氢氧化铁沉淀,铝离子与氢氧根离子结合成偏铝酸根和水,离子方程式为Fe3++3OH-=Fe(OH)3↓、Al3++4OH-=AlO2-+2H2O,
故答案为:Fe3++3OH-=Fe(OH)3↓、Al3++4OH-=AlO2-+2H2O;
(4)AlCl3是强酸弱碱盐,结晶过程中会发生水解,为了防止其发生水解,可在HCl气流中加热脱结晶水,
故答案为:HCl;
(5)2Al2O 3
4Al+3O2,转移电子的物质的量等于生成铝的物质的量的3倍,2.7吨铝Al的物质的量为100mol,转移电子数为100×3NA=300NA,
故答案为:300.
| ||
故答案为:A12O3+3C12+3C
| ||
(2)Cl2有强氧化性,将SO32-氧化为SO42-,自身被还原为2C1-.反应离子方程式为SO32-+C12+H2O═SO42-+2C1-+2H+,
故答案为:SO32-+C12+H2O═SO42-+2C1-+2H+;
(3)无水AlCl3产品(含杂质FeCl3),溶于过量NaOH溶液过程中,铁离子与氢氧根离子结合成氢氧化铁沉淀,铝离子与氢氧根离子结合成偏铝酸根和水,离子方程式为Fe3++3OH-=Fe(OH)3↓、Al3++4OH-=AlO2-+2H2O,
故答案为:Fe3++3OH-=Fe(OH)3↓、Al3++4OH-=AlO2-+2H2O;
(4)AlCl3是强酸弱碱盐,结晶过程中会发生水解,为了防止其发生水解,可在HCl气流中加热脱结晶水,
故答案为:HCl;
(5)2Al2O 3
| ||
| 电解,冰晶石 |
故答案为:300.
点评:本题考查了无水AlCl3的工艺制备,涉及离子方程式书写、电解原理、转移电子数的计算等,难度一般,培养了学生运用分析、比较、归纳等方法对所获取的信息进行初步加工和应用的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
向明矾[KAl(SO4)2?12H2O]溶液中滴加Ba(OH)2溶液,当SO42-完全沉淀时,铝元素的存在形式是( )
| A、全部为Al(OH)3沉淀 |
| B、几乎全部以[Al(OH)4]-形式存在于溶液中 |
| C、一部分为Al(OH)3沉淀,一部分以Al3+存在于溶液中 |
| D、一部分为Al(OH)3沉淀,一部分以[Al(OH)4]-形式存在于溶液中 |
在下列反应中,aXO4-+bY-+cH+═dX2++eY2+8H2O,化学计量数b,d分别为( )
| A、5,6 | B、10,2 |
| C、6,2 | D、10,5 |
现有
X和
X+两种粒子,下列叙述正确的是( )
A Z |
A+1 Z |
A、
| ||
| B、X元素的质量数为A | ||
| C、质子数相等 | ||
| D、它们的化学性质几乎完全相同 |
下列说法中,不正确的是( )
| A、李比希燃烧法、钠熔法、铜丝燃烧法、纸层析法都是元素定性分析法 |
| B、红外光谱分析法常用来判断有机化合物中具有哪些基团 |
| C、麦芽糖、乳糖、纤维二糖互为同分异构体,分子式都为C12H22O11 |
| D、绿色荧光蛋白质(GFP)是高分子化合物,其水溶液有丁达尔效应 |
下列有关实验的叙述正确的是( )
| A、已知Cu2O+2H+═Cu2++Cu+H2O,氢气还原氧化铜后生成的红色固体能完全溶于稀硝酸,说明还原产物是铜 |
| B、在中和热测定的实验中,将NaOH溶液和盐酸混合反应后的冷却温度作为末温度 |
| C、仅用淀粉溶液、稀硫酸、碘水、新制氢氧化铜四种试剂可完成淀粉水解产物及水解程度检验的探究实验 |
| D、向盛有少量Mg(OH)2悬浊液的试管中滴加氯化铵溶液,可以看到沉淀溶解 |
向一定量的Fe、FeO、Fe2O3的混合物中加入100ml浓度为1mol/L的硫酸,恰好使混合物完全溶解,放出标况下224ml的气体.所得溶液中加入KSCN溶液后无血红色出现.若用足量的H2在高温下还原相同质量的此混合物,能得到铁的质量是( )
| A、11.2g | B、5.6g |
| C、2.8g | D、1.4g |
一定条件下,容积为2L的恒容密闭容器中,通入2mol N2、3mol H2进行反应催化剂高温高压N2(g)+3H2(g)?2NH3(g),20min后,N2的物质的量为1.9mol,1h后测得容器内气体的压强不再改变,且为反应开始时压强的0.8倍,则下列叙述正确的是( )
| A、1 h后反应进行完全,容器中的N2浓度为0.55 mol?L-1 |
| B、前20 min用NH3表示的反应速率为0.01 mol?L-1?min-1 |
| C、增加H2的浓度或降低温度,平衡将向正反应方向移动,且反应速率均加快 |
| D、当容器内压强不改变时,说明反应已达到平衡状态 |