题目内容
下列说法正确的是
A.25 ℃时、用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH
B.饱和小苏打溶液中:c(Na+)=c(HCO3-)
C.Na2CO3溶液中加入少量Ca(OH)2 固体,CO32-水解程度减小,溶液的pH 减小
D.室温下,对于0.10 mol·L-1的氨水,用HNO3溶液完全中和后,溶液不显中性
D
【解析】
试题分析:A.若恰好反应生成强碱弱酸盐,因PH=7,说明醋酸体积略大,错误;B.小苏打是强碱弱酸盐,碳酸氢根离子会因水解而减小,错误;C.碳酸根离子与钙离子反应,导致CO32-水解程度减小,但溶液的pH 增大,错误;D.两溶液恰好反应,生成强酸弱碱盐,显酸性,正确;选D。
考点:考查中和滴定,溶液中离子浓度大小比较等知识。

练习册系列答案
相关题目
 2 C(g),经2s后测得C的浓度为0.6 mol·L-1,下列几种说法中正确的是
2 C(g),经2s后测得C的浓度为0.6 mol·L-1,下列几种说法中正确的是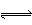 H+ + Cl– + HClO
H+ + Cl– + HClO