题目内容
下列各组物质中属于同分异构体的是( )
| A、金刚石和C60 |
B、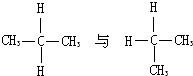 |
C、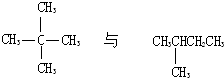 |
| D、CH4与CH3CH3 |
考点:有机化合物的异构现象
专题:同分异构体的类型及其判定
分析:同素异形体是同种元素形成的不同单质;
具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素;
有机化合物中具有同一通式、组成上相差一个或多个CH2原子团、在结构与性质上相似的化合物互为同系物;
具有相同分子式而结构不同的化合物互为同分异构体;
根据以上概念进行判断.
具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素;
有机化合物中具有同一通式、组成上相差一个或多个CH2原子团、在结构与性质上相似的化合物互为同系物;
具有相同分子式而结构不同的化合物互为同分异构体;
根据以上概念进行判断.
解答:
解:A.金刚石和C60:二者为碳元素的不同单质,互为同素异形体,故A错误;
B.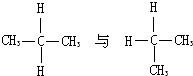 :丙烷不存在同分异构体,二者为同一种物质,故B错误;
:丙烷不存在同分异构体,二者为同一种物质,故B错误;
C.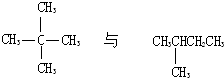 二者分别为新戊烷和异戊烷,都是戊烷的同分异构体,故C正确;
二者分别为新戊烷和异戊烷,都是戊烷的同分异构体,故C正确;
D.CH4与CH3CH3:甲烷和乙烷都属于烷烃,为烷烃的同系物,故D错误;
故选C.
B.
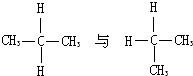 :丙烷不存在同分异构体,二者为同一种物质,故B错误;
:丙烷不存在同分异构体,二者为同一种物质,故B错误;C.
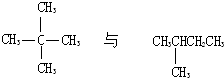 二者分别为新戊烷和异戊烷,都是戊烷的同分异构体,故C正确;
二者分别为新戊烷和异戊烷,都是戊烷的同分异构体,故C正确;D.CH4与CH3CH3:甲烷和乙烷都属于烷烃,为烷烃的同系物,故D错误;
故选C.
点评:本题考查了同分异构体的判断,题目难度不大,试题侧重基础知识的考查,注意掌握同分异构体的概念及判断方法,明确同系物、同分异构体、同素异形体、同位素等概念的区别.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
在25℃时浓度分别为a、b、c(mol/L)的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2(硫酸亚铁铵)三种溶液中,测得其中NH4+的物质的量的浓度相等,则下列判断正确的是( )
| A、a>b>c |
| B、c>a>b |
| C、a>c>b |
| D、b>a>c |
下列有机物,既能被酸性高锰酸钾溶液氧化,又能与溴水发生加成反应的是( )
| A、苯 | B、甲苯 | C、乙烯 | D、乙烷 |
已知空气-锌电池的电极反应:锌片:Zn-2OH--2e-═ZnO+H2O,石墨:
O2+H2O+2e-═2OH-据次推断锌片是( )
| 1 |
| 2 |
| A、负极,被氧化 |
| B、负极,被还原 |
| C、正极,被氧化 |
| D、正极,被还原 |
PCl3和PCl5都是重要的化工原料.将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中,在一定条件下发生下述反应,并于10min时达到平衡:PCl3(g)+Cl2(g)?PCl5(g).有关数据如下:
下列判断不正确的是( )
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度/(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度/(mol/L) | c1 | c2 | 0.4 |
| A、10min内,v(Cl2)=0.04mol/(L?min) |
| B、当反应达到平衡时,容器中Cl2为1.2mol |
| C、升高温度,反应的平衡常数减小,则平衡时PCl3的转化率变大 |
| D、平衡后移走2.0mol PCl3和1.0mol Cl2,在相同条件下再达平衡时,c(PCl5)=0.2mol/L |
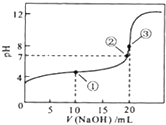 常温下,用0.1000mol/LNaOH溶液滴定20.00mL0.1000mol/LHCl溶液,滴定曲线如图所示,下列说法正确的是( )
常温下,用0.1000mol/LNaOH溶液滴定20.00mL0.1000mol/LHCl溶液,滴定曲线如图所示,下列说法正确的是( )| A、a=20.0 |
| B、滴定过程中,不可能存在:c(Cl-)>c(H)+>c(Na+)>c(OH-) |
| C、若用酚酞作指示剂,当滴定到溶液明显由无色变为红色时停止滴定 |
| D、若将盐酸换作同浓度的醋酸,则滴定到pH=7时,a>20.00 |
-定条件下,2SO2(g)+O2(g)?2SO2(g)△H<0.下列有关叙述正确的是( )
| A、升髙温度,v正变大,v逆变小 |
| B、恒温恒容,充入O2,02的转化率升高 |
| C、恒温恒压,充人N2,平衡不移动 |
| D、恒温恒容,平衡前后混合气体的密度保持不变 |