题目内容
(1)在标准状况下,200mL某气体的质量为1.142g,该气体的摩尔质量为
(2)已知某种混盐中含Na+、Mg2+、K+和Cl-离子物质的量分别为0.80mol、0.05mol、0.20mol和0.90mol.测知该混盐中还有SO42-,则SO42-物质的量为
(3)实验分析得知,200mL某硫酸铝溶液中含Al3+0.54g,求该溶液中硫酸根的物质的量浓度.
(2)已知某种混盐中含Na+、Mg2+、K+和Cl-离子物质的量分别为0.80mol、0.05mol、0.20mol和0.90mol.测知该混盐中还有SO42-,则SO42-物质的量为
(3)实验分析得知,200mL某硫酸铝溶液中含Al3+0.54g,求该溶液中硫酸根的物质的量浓度.
考点:物质的量的相关计算
专题:计算题
分析:(1)根据n=
计算气体的物质的量,再根据M=
计算其摩尔质量;
(2)溶液呈电中性,根据电荷守恒有:n(Na+)+2n(Mg2+)+n(K+)+n(Cl-)+2n(SO42-),据此解答;
(3)根据n=
计算Al3+的物质的量,溶液中2n(SO42-)=3n(Al3+),再根据c=
计算SO42-的物质的量浓度.
| V |
| Vm |
| m |
| n |
(2)溶液呈电中性,根据电荷守恒有:n(Na+)+2n(Mg2+)+n(K+)+n(Cl-)+2n(SO42-),据此解答;
(3)根据n=
| m |
| M |
| n |
| V |
解答:
解:(1)200mL气体的物质的量为
=
mol,其摩尔质量为
=128g/mol,故答案为:128g/mol;
(2)溶液呈电中性,根据电荷守恒有:n(Na+)+2n(Mg2+)+n(K+)+n(Cl-)+2n(SO42-),即:0.8mol+0.05mol×2+0.20mol=0.90mol+2n(SO42-),解得n(SO42-)=0.1mol,故答案为:0.1mol;
(3)Al3+的物质的量为
=0.02mol,溶液中2n(SO42-)=3n(Al3+),则SO42-的物质的量为0.02mol×
=0.03mol,SO42-的物质的量浓度为
=0.15mol/L,
答:SO42-的物质的量浓度为0.15mol/L.
| 0.2L |
| 22.4L/mol |
| 0.2 |
| 22.4 |
| 1.142g | ||
|
(2)溶液呈电中性,根据电荷守恒有:n(Na+)+2n(Mg2+)+n(K+)+n(Cl-)+2n(SO42-),即:0.8mol+0.05mol×2+0.20mol=0.90mol+2n(SO42-),解得n(SO42-)=0.1mol,故答案为:0.1mol;
(3)Al3+的物质的量为
| 0.54g |
| 27g/mol |
| 3 |
| 2 |
| 0.03mol |
| 0.2L |
答:SO42-的物质的量浓度为0.15mol/L.
点评:本题考查物质的量有关计算,难度不大,注意(2)中电解质混合溶液中离子物质的量计算经常利用电荷守恒计算.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、1.0mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B、含有大量Fe2+的溶液中:H+、Mg2+、ClO-、NO3- |
| C、c(H+)=10-12mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
| D、能使Al溶解产生H2的溶液中:NH4+、Na+、SiO32-、HCO3- |
下列反应中属于氧化还原反应,伹水既不作氧化剂又不作还原剂的是( )
| A、SO3+H2O=H2SO4 |
| B、Cl2+H2O=HCl+HClO |
| C、2F2+2H2O=4HF+O2 |
| D、2Na+2H2O=2NaOH+H2↑ |
下列有关能源与能量的说法正确的是( )
| A、煤和石油是经过亿万年形成的,亿万年后煤和石油还会生成,故二者属可再生能源 |
| B、蒸汽属于一次能源 |
| C、凡经过加热而发生的反应都是吸热反应,常温下进行的反应都是放热反应 |
| D、反应物和生成物的总能量决定反应是放热还是吸热 |
质子数和中子数相同的原子A,其阳离子An+核外共有x个电子,则A的质量数为( )
| A、2(x+n) | B、2(x-n) |
| C、2x | D、n+2x |
深秋雨后的清晨,我们常会遇到大雾天气,雾中小液滴直径范围是( )
| A、小于1 nm |
| B、在1~100 nm间 |
| C、大于100 nm |
| D、无法确定 |
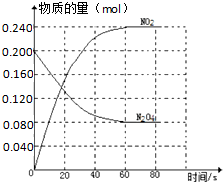 在容积固定为2.00L的密闭容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g)△H>0,100℃时体系中各物质的量(mol)随时间变化如图所示( )
在容积固定为2.00L的密闭容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g)△H>0,100℃时体系中各物质的量(mol)随时间变化如图所示( )| A、100℃时,在0-60s时段反应的平均反应速率v(N2O4)=0.002mol/(L?s) |
| B、100℃时,反应的平衡常数K为0.72mol?L-1 |
| C、100℃时达到平衡后,其它条件不变,仅改变反应温度为T,N2O4以0.001mol/(L?s)的平均速率变化,经10s又达到平衡,则T大于100℃ |
| D、保持反应体系的温度不变(100℃),再向该平衡体系中再加入一定量的N2O4,重新达平衡后,N2O4的体积分数与原平衡相等 |
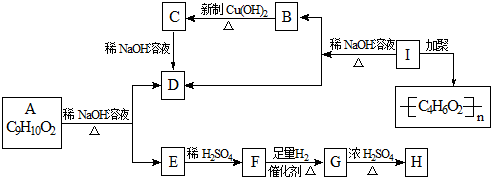
 .化学式为C9H10O2的有机物A有如下的转化关系:
.化学式为C9H10O2的有机物A有如下的转化关系: