题目内容
11.肼(N2H4)-空气燃料电池是一种环保型碱性燃料电池,电解质为20%~30%的KOH溶液,电池总反应为:N2H4+O2═N2+2H20.下列关于该电池工作时说法中正确的是( )| A. | 正极的电极反应式为:O2+4H++4e-═2H2O | |
| B. | 溶液中阴离子向正极移动 | |
| C. | 负极的电极反应式为:N2H4+4OH--4e-═4H2O+N2 | |
| D. | 电解质溶液的pH保持不变 |
分析 肼(N2H4)一空气燃料电池中,负极反应为:N2H4+4OH--4e-=4H2O+N2↑,正极反应为:O2+2H2O+4e-=4OH-,电池总反应为:N2H4+O2=N2↑+2H2O,以此解答题中A、B、C各问,原电池中,阴离子向负极移动,阳离子向正极移动.
解答 解:A、在碱性环境下,正极反应为:O2+2H2O+4e-=4OH-,故B错误;
B、原电池中,阴离子向负极移动,阳离子向正极移动,故C错误;
C、原电池中负极发生氧化反应,正极发生还原反应,负极反应为N2H4+4OH--4e-=4H2O+N2↑,故C正确;
D、电池总反应为N2H4+O2=N2↑+2H2O,原电池反应生成水,溶液浓度降低,电解质溶液的pH降低,故D错误;
故选C.
点评 本题考查原电池的工作原理,题目难度不大,本题注意把握电极反应式的书写,正确判断离子的定向移动.

练习册系列答案
相关题目
1.某混合溶液中可能含有下列离子中的若干种:Na+、K+、Fe2+、Fe3+、SO42-、CO32- 现取三份该溶液进行如下实验:
(1)第一份加入足量盐酸,无任何气体产生;
(2)第二份加入足量NaOH溶液,经搅拌、过滤、洗涤、灼烧、最后得到红棕色固体;
(3)第三份滴加0.1mol.L-1酸性KMnO4溶液,KMnO4溶液的紫色消失
(4)另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色.
根据上述实验,以下说法正确的是( )
(1)第一份加入足量盐酸,无任何气体产生;
(2)第二份加入足量NaOH溶液,经搅拌、过滤、洗涤、灼烧、最后得到红棕色固体;
(3)第三份滴加0.1mol.L-1酸性KMnO4溶液,KMnO4溶液的紫色消失
(4)另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色.
根据上述实验,以下说法正确的是( )
| A. | 原混合溶液中只存在Na+、Fe3+、SO42-,不可能存在K+、CO32- | |
| B. | 由实验(1)无法推断原混合溶液中是否含有SO42- | |
| C. | 由实验(2)无法推断原混合溶液中是否含有Fe3+ | |
| D. | 由实验(3)可推断原混合溶液中存在Fe2+ |
19.下列物质属于碱性氧化物的是( )
| A. | CO2 | B. | CaO | C. | Na2O2 | D. | Al2O3 |
6.实验是研究化学的基础,如图装置或操作正确的是( )
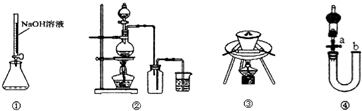

| A. | 用装置①量取15.00mL的NaOH溶液 | |
| B. | 用装置②制备并收集Cl2 | |
| C. | 用装置③陶瓷坩埚高温煅烧CaCO3固体 | |
| D. | 关闭活塞a,从b处加水,以检查装置④的气密性 |
16.某一海水资源利用的原理如图所示,下列有关说法正确的是( )
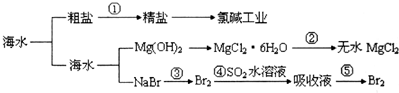

| A. | 第①步中除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 | |
| B. | 工业上金属钠是通过氯碱工业制取的 | |
| C. | ④和⑤步的目的是为了浓缩 | |
| D. | 第③④⑤步中溴元素均被氧化 |
20.食盐、食醋、纯碱等都是厨房常用的物质,其中属于盐的是( )
| A. | 食盐和食醋 | B. | 食盐和纯碱 | C. | 纯碱和食醋 | D. | 全部 |
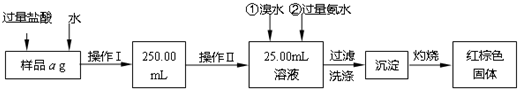
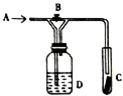 如图是一种试验某气体化学性质的实验装置,图中B为弹簧夹.在A处通入未经干燥的氯气,当打开弹簧夹B时,C中红色布条颜色褪去;当关闭弹簧夹B时,C中红色布条颜色无变化.则D瓶所盛的溶液是( )
如图是一种试验某气体化学性质的实验装置,图中B为弹簧夹.在A处通入未经干燥的氯气,当打开弹簧夹B时,C中红色布条颜色褪去;当关闭弹簧夹B时,C中红色布条颜色无变化.则D瓶所盛的溶液是( )