��Ŀ����
4��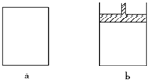 ��a��b���������ȵ��ܱ�������a�����ݻ����䣬b�еĻ����������ƶ����Ա�������ѹǿ��ȣ�����ͬ�����½�3molA��1molB�ֱ�ͬʱ�����a��b�������У�������Ӧ��
��a��b���������ȵ��ܱ�������a�����ݻ����䣬b�еĻ����������ƶ����Ա�������ѹǿ��ȣ�����ͬ�����½�3molA��1molB�ֱ�ͬʱ�����a��b�������У�������Ӧ��3A��g��+B��g��?2C��g��+D��g��
��1����ƽ��ʱ��a��A��Ũ��ΪM mol?L-1��C��Ũ��ΪN mol?L-1��b��A��Ũ��Ϊm mol?L-1��C��Ũ��Ϊn mol?L-1����M��m��N��n�� �������������=�������Ƚϡ���
��2�������¶Ȳ��䣬��������ȷֱ���� a��b ����������ƽ���a��C��Ũ��ΪN mol?L-1����DE��b��C��Ũ��Ϊn mol?L-1����ADE
A.6molA+2molB B.3molA+2molC C.2molC+1molB+1mol D
D.2molC+1molD E.1.5molA+0.5molB+1molC+0.5molD
��3������2molC��2molD����a�У������¶Ȳ��䣬ƽ��ʱA��Ũ��ΪWmol?L-1��C��Ũ��ΪYmol?L-1����W��M��Y��N֮��Ĺ�ϵΪW��M��Y��N�� ���������=�����Ƚϣ�
��4�������¶Ȳ��䣬����4molC��2molD����a�У�ƽ��ʱA��Ũ��ΪR mol?L-1�����ϵʽ��ȷ����C
A��R=2M B��R��M C��M��R��2M D��R��2M��
���� ��1��a�����ݻ����䣬b��������ѹǿ��ȣ���Ӧ3A��g��+B��g��?2C��g��+D��g�����������ʵ������ٵķ�Ӧ��ƽ��ʱa��ѹǿ��b��С����b�൱����aƽ��Ļ����ϼ�ѹ��ƽ�����ƣ�ƽ���ƶ���������A��Ũ����������ƽ��ʱ��Ũ�ȸ���ԭƽ�⣻
��2���ı���ʼͶ�ϱȣ�Ҫ��ﵽƽ���a��C��Ũ����ΪN mol•L-1�����º����£���ԭƽ������ȫ��Чƽ�⣬����ѧ������ת��������ʽ��ߣ�������ԭƽ������ͬ���ʵ���ʼͶ������ȣ�
b��C��Ũ��Ϊn mol•L-1����ԭƽ��Ϊ��Чƽ�⣬���µ�ѹ�������£�����ѧ������ת��������ʽ��ߣ�������ԭƽ�������ʵ�Ͷ�����ȣ�
��3������2molC��2molD����a�У���ЧΪ��ʼͶ��3molA��g����1molB��g����1molD��g������ԭƽ�����ƽ�������ƶ���
��4����4 mol C��2 mol D����a���൱�ڿ�ʼ����6 mol A��2 mol B��ѹǿ����ƽ�������ƶ�����Ӧ��ת�������μӷ�Ӧ��A�����ʵ�������ԭƽ���2����ƽ���ƶ���������A��Ũ����������ƽ��ʱ��Ũ�ȸ���ԭƽ�⣮
��� �⣺��1��a�����ݻ����䣬b��������ѹǿ��ȣ���Ӧ3A��g��+B��g��?2C��g��+D��g�����������ʵ������ٵķ�Ӧ��ƽ��ʱa��ѹǿ��b��С����b�൱����aƽ��Ļ����ϼ�ѹ��ƽ�����ƣ�ƽ���ƶ���������A��Ũ����������ƽ��ʱ��Ũ�ȸ���ԭƽ�⣬��b��ƽ��ʱA��Ũ�ȴ���a��A��ƽ��Ũ�ȣ���M��m��ƽ�����ƣ�b��C��ƽ��Ũ�ȸ���a��C��ƽ��Ũ�ȣ���N��n��
�ʴ�Ϊ����������
��2���ı���ʼͶ�ϱȣ�Ҫ��ﵽƽ���a��C��Ũ����ΪN mol•L-1�����º����£���ԭƽ������ȫ��Чƽ�⣬����ѧ������ת��������ʽ��ߣ�������ԭƽ������ͬ���ʵ���ʼͶ������ȣ�ѡ����DE���ϣ�
b��C��Ũ��Ϊn mol•L-1����ԭƽ��Ϊ��Чƽ�⣬���µ�ѹ�������£�����ѧ������ת��������ʽ��ߣ�������ԭƽ�������ʵ�Ͷ�����ȣ�ѡ����ADE���ϣ�
�ʴ�Ϊ��DE��ADE��
��3������2molC��2molD����a�У���ЧΪ��ʼͶ��3molA��g����1molB��g����1molD��g������ԭƽ�����ƽ�������ƶ�����ƽ��ʱA��Ũ������C��Ũ�ȼ�С����W��M��Y��N��
�ʴ�Ϊ����������
��4����4mol C��2 mol D����a���൱�ڿ�ʼ����6 mol A+2 mol B��ѹǿ����ƽ�������ƶ�����Ӧ��ת�������μӷ�Ӧ��A�����ʵ�������ԭƽ���2����ƽ��ʱA��Ũ��С��ԭƽ���2����ƽ���ƶ���������A��Ũ����������ƽ��ʱ��Ũ�ȸ���ԭƽ�⣬��M��R��2M��
�ʴ�Ϊ��C��
���� ���⿼�黯ѧƽ���ƶ�����㣬Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬�Ѷ��еȣ�ע�����õ�Ч˼�����ƽ�⽨����;���������Чƽ����ɣ�1�����º��ݣ���Ӧǰ������������ȣ�����ѧ������ת����һ�ߣ���Ӧ���������������Ӧǰ�����������ȣ�����ѧ������ת����һ�ߣ���Ӧ��������ȱȣ�2�����º�ѹ������ѧ������ת����һ�ߣ���Ӧ��������ȱȣ�

 ֥�鿪���γ�������ϵ�д�
֥�鿪���γ�������ϵ�д�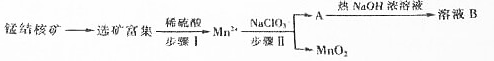
�������ݵĵ����Ũ�Ȼ�������Ksp�����±���
| ������ | Zn��OH��2 | Fe��OH��2 | Fe��OH��3 |
| Ksp����ֵ | 10-17 | 10-17 | 10-39 |
��1�������������0.5molMn2+ʱ����ȥ1mol•L-1��NaClO3��Һ200mL���÷�Ӧ���ӷ���ʽΪ2ClO3-+5Mn2++4H2O=5MnO2+8H++Cl2��
��2����֪��ҺB������֮һ��ѭ���������������������ʵ�������������
��3��MnO2�Ǽ���п�̵�ص��������ϣ��ŵ���̲���MnOOH���õ�������ĵ缫��Ӧʽ��MnO2+H2O+e-�TMnOOH+OH-�����ά�ֵ���ǿ��Ϊ5A����ع���5���ӣ���������п0.5g����֪F=96500C/mol��
��4����Ͼ�п�̵���ڵĻ�����Ҫ�ɷ�MnOOH��Zn��OH��2���м���һ������ϡ�����ϡ���ᣨH2C2O4���������Ͻ�������CO2����Ϊֹ��д��MnOOH���뷴Ӧ�����ӷ���ʽΪ2MnOOH+H2C2O4+2H2SO4=2CO2��+2MnSO4+4H2O����������Һ�еμӸ��������Һ������ɫ���������ʵ��֤����ɫ�¶��ɷ�ΪMnO2ȡ������ɫ��������Թ��У���������Ũ���Ტ���ȣ���������ɫ���壬˵����ɫ����ΪMnO2
��5���÷Ͼɵ�ص�пƤ����ZnSO4•7H2O�Ĺ����У����ȥпƤ�����������������䷽���ǣ�����ϡH2SO4��H2O2�����ܽ��ΪFe3+���Ӽ��pHΪ2.7ʱ�����պó�����ȫ������Ũ��С��1��10-5mol•L-1ʱ��������Ϊ�����ӳ�����ȫ������������pHΪ6ʱ��п��ʼ�������ٶ�Zn2+Ũ��Ϊ0.1mol•L-1�������������̲���H2O2��������ԭ����Zn��OH��2��Fe��OH��2��Ksp�����Zn2+��Fe2+���벻����
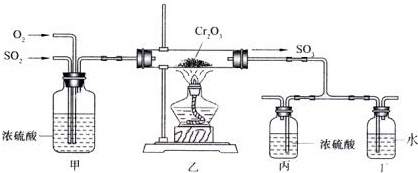
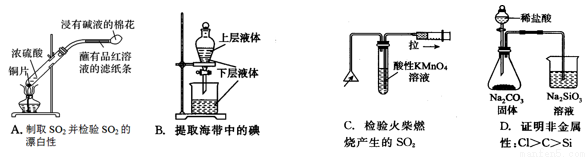
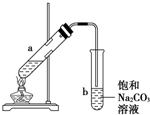 ��ͼΪʵ������ȡ��������������װ��ͼ�����й��ڸ�ʵ��������У�����ȷ���ǣ�������
��ͼΪʵ������ȡ��������������װ��ͼ�����й��ڸ�ʵ��������У�����ȷ���ǣ�������| A�� | ��a�Թ����ȼ����Ҵ���Ȼ���ҡ���Թܱ���������Ũ���ᣬ�ټӱ����� | |
| B�� | �Թ�b�е������¶˹ܿڲ��ܽ���Һ���ԭ���Ƿ�ֹʵ������з����������� | |
| C�� | ʵ��ʱ�����Թ�a��Ŀ���Ǽ�ʱ�����������������ӿ췴Ӧ���� | |
| D�� | �ɽ�����̼������Һ��������������Һ |
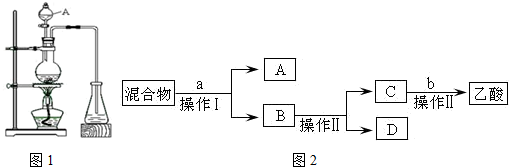
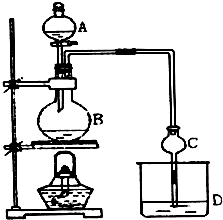 ij����С����Ƶ�ʵ������ȡ����������װ����ͼ��ʾ��A�з���Ũ���ᣬB�з����Ҵ�����ˮ�����ƣ�D�з��б���̼������Һ��
ij����С����Ƶ�ʵ������ȡ����������װ����ͼ��ʾ��A�з���Ũ���ᣬB�з����Ҵ�����ˮ�����ƣ�D�з��б���̼������Һ����֪������ˮ�Ȼ��ƿ����Ҵ��γ�������ˮ��CaCl2•6C2H5OH��
���й��л���ķе㣺
| �Լ� | ���� | �Ҵ� | ���� | �������� |
| �е㣨�棩 | 34.7 | 78.5 | 118 | 77.1 |
 CH3CO18OC2H5+H2O��
CH3CO18OC2H5+H2O����2�����θ����C�������Ƿ�ֹ��������������ϸ�۲���ҺD�л����������ݲ������������ӷ���ʽ���Ͳ����������ԭ����2CH3COOH+CO32-=2CH3COO-+CO2��+H2O��
��3����ʵ������۲췢��װ��B����Һ������غ�ɫ�����û�ѧ����ʽ������ԭ��C2H5OH+2H2SO4��2C+2SO2��+5H2O��
��4����D�з���������������г�����һ�������Ҵ������Ѻ�����ˮ��Ӧ�ȼ�����ˮ�Ȼ��ƣ�������Ҵ���Ȼ���ڻ��Һ�м����ʯ���ټ��Ƚ��������ռ�77.1�� ���ҵ���֣��Եýϴ���������������
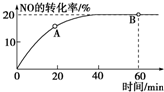 ��1��ij�¶��£����ݻ�Ϊ1L�������г���3mol NO��1mol CO������2NO��g��+2CO��g��???N2��g��+2CO2��g����Ӧ��NO��ת������ʱ��ı仯��ͼ��ʾ��
��1��ij�¶��£����ݻ�Ϊ1L�������г���3mol NO��1mol CO������2NO��g��+2CO��g��???N2��g��+2CO2��g����Ӧ��NO��ת������ʱ��ı仯��ͼ��ʾ��