题目内容
3.下列实验中不能观察到明显现象的是( )| A. | 少量的氯水加入到盛有NaBr溶液的试管中 | |
| B. | 取一小片铝,砂纸除去氧化膜,放入试管中,加入少量2mL水 | |
| C. | 将锌片与铜片用导线连接,插入盛稀硫酸的烧杯中 | |
| D. | 向盛有过氧化氢水溶液的试管中,加入少量1mol/LFeCl3溶液 |
分析 A.氯水中的氯气具有氧化性能氧化溴离子生成溴单质;
B.常温下铝和水不反应;
C.将锌片与铜片用导线连接,插入盛稀硫酸溶液中选出原电池,铜片上冒气泡;
D.氯化铁对过氧化氢分解起到催化剂的作用反应速率加快;
解答 解:A.氯水中的氯气具有氧化性能氧化溴离子生成溴单质,Cl2+2Br-=Br2+2Cl-,溴单质溶于水溶液呈橙红色,能观察到明显现象,故A错误;
B.在持续加热条件下铝和水反应生成氢氧化铝和氢气,常温下铝和水不反应,不能观察到明显现象,故B正确;
C.将锌片与铜片用导线连接,插入盛稀硫酸溶液中选出原电池,铜片上冒气泡,锌片质量减少,故C错误;
D.过氧化氢分解生成水和氧气,氯化铁对过氧化氢分解起到催化剂的作用反应速率加快,故D错误;
故选B.
点评 本题考查了氯气、铝、过氧化物、氯化铁的性质、原电池反应等知识点,掌握基础是解题关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.化学源于生活,同时又服务于生活.以下做法不合理的是( )
| A. | 用食醋除去暖水瓶中的薄层水垢 | |
| B. | 一般不用纯碱代替小苏打作食品发酵粉 | |
| C. | 用甲醛溶液浸泡海产品以保鲜 | |
| D. | 用灼烧并闻气味的方法区别纯棉织物和纯毛织物 |
14.用中和滴定法测定烧碱的纯度(烧碱中的杂质不和酸反应),请根据实验回答:
(1)将已称量好的8.8g烧碱样品配制成500mL待测液,配制过程使用的主要仪器除 500mL容量瓶、量筒、烧杯、胶头滴管外,还有一种必须使用的仪器是玻璃棒;
(2)用碱式滴定管量取10.00mL待测液于锥形瓶中,滴入几滴酚酞;
(3)用0.20mol•Lˉ1的标准盐酸滴定待测液,判断滴定终点的现象是:当滴入最后一滴盐酸,溶液由红色变为无色,且半分钟内不褪色;
(4)经过分析发现,本次实验的测定结果比烧碱的实际纯度偏高,造成误差的可能原因是BCDF;
A.滴定前平视,滴定后俯视
B.未用标准液润洗滴定管
C.用待测液润洗锥形瓶
D.不小心将标准液滴在锥形瓶外面
E.滴定接近终点时,用少量蒸馏水冲洗锥形瓶内壁
F.滴定前尖嘴有气泡,滴定后消失
(5)根据下列数据计算,烧碱的纯度为91%(保留整数).
(1)将已称量好的8.8g烧碱样品配制成500mL待测液,配制过程使用的主要仪器除 500mL容量瓶、量筒、烧杯、胶头滴管外,还有一种必须使用的仪器是玻璃棒;
(2)用碱式滴定管量取10.00mL待测液于锥形瓶中,滴入几滴酚酞;
(3)用0.20mol•Lˉ1的标准盐酸滴定待测液,判断滴定终点的现象是:当滴入最后一滴盐酸,溶液由红色变为无色,且半分钟内不褪色;
(4)经过分析发现,本次实验的测定结果比烧碱的实际纯度偏高,造成误差的可能原因是BCDF;
A.滴定前平视,滴定后俯视
B.未用标准液润洗滴定管
C.用待测液润洗锥形瓶
D.不小心将标准液滴在锥形瓶外面
E.滴定接近终点时,用少量蒸馏水冲洗锥形瓶内壁
F.滴定前尖嘴有气泡,滴定后消失
(5)根据下列数据计算,烧碱的纯度为91%(保留整数).
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.60 | 20.50 |
| 第二次 | 10.00 | 3.00 | 23.10 |
8. 欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol•L-1HCl标准溶液进行中和滴定(用酚酞作指示剂).请回答下列问题:
欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol•L-1HCl标准溶液进行中和滴定(用酚酞作指示剂).请回答下列问题:
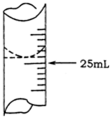
(1)若甲同学在实验过程中,记录滴定前滴定管内液面读数为1.10mL,滴定后液面如图,则此时消耗HCl标准溶液的体积为23.80mL.
(2)乙学生做了2组平行实验,数据记录如下:
据此计算出待测NaOH溶液的物质的量浓度为0.0800 mol•L-1(小数点后保留四位);乙同学判断达到滴定终点时的现象为滴入最后一滴盐酸,溶液有红色变为无色,且半分钟不恢复红色.
 欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol•L-1HCl标准溶液进行中和滴定(用酚酞作指示剂).请回答下列问题:
欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol•L-1HCl标准溶液进行中和滴定(用酚酞作指示剂).请回答下列问题:(1)若甲同学在实验过程中,记录滴定前滴定管内液面读数为1.10mL,滴定后液面如图,则此时消耗HCl标准溶液的体积为23.80mL.
(2)乙学生做了2组平行实验,数据记录如下:
| 实验序号 | 待测NaOH溶液的体积/mL | HCl标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 20.10 |
| 2 | 25.00 | 1.50 | 21.40 |
15.跟氨分子所含的质子总数和电子总数都相同的粒子是( )
| A. | Na+ | B. | Mg2+ | C. | HCl | D. | HF |
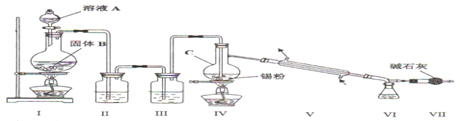
 阅读下列实验内容,根据题目要求回答问题:
阅读下列实验内容,根据题目要求回答问题: