题目内容
15.标准状况下,下列关于等质量H2、D2、T2三种气体的叙述不正确的是( )| A. | 相对分子质量之比1:2:3 | B. | 质子数之比2:3:6 | ||
| C. | 电子数之比为6:3:2 | D. | 体积之比6:3:2 |
分析 A.H2、D2、T2相对分子质量分别为:2;4;6;
B.同位素含有相同的质子数;
C.分子呈电中性,分子中质子数=电子数;
D.相同状况下,气体体积之比等于物质的量之比.
解答 解:A.H2、D2、T2相对分子质量分别为:2;4;6,相对分子质量之比1:2:3,故A正确;
B.每个H2、D2、T2分子中都含有2个质子,等质量H2、D2、T2三种气体的物质的量之比为6:3:2,所以含有的质子数之比为6:3:2,故B错误;
C.分子呈电中性,分子中质子数=电子数,参照B可知,等质量H2、D2、T2三种气体的物质的量之比为6:3:2,所以含有的电子数之比为6:3:2,故C正确;
D.相同状况下,气体体积之比等于物质的量之比,等质量H2、D2、T2三种气体物质的量之比为6:3:2,所以相同条件下,体积之比为:6:3:2,故D正确;
故选:B.
点评 本题考查原子的构成及有关阿伏伽德罗常数的相关计算,依据明确H2、D2、T2相对分子质量,熟悉分子中质子、电子数之间关系是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列离子方程式正确的是( )
| A. | 高锰酸钾溶液与乙二酸(草酸)反应:2MnO4-+5C2O42-+16H+→2Mn2++10CO2↑+8H2O | |
| B. | 苯酚与碳酸钠溶液: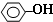 +CO32-→ +CO32-→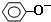 +H2CO3 +H2CO3 | |
| C. | 等体积等物质的量浓度的NH4Fe(SO4)2和Ba(OH)2混合:2Fe3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Fe(OH)3↓ | |
| D. | 在强碱性溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
6.下列物质属于纯净物的是( )
| A. | 汽油 | B. | 红酒 | C. | 干冰 | D. | 碘酒 |
10.将淀粉浆和淀粉酶的混合物放在半透膜袋中,扎好袋口,浸入流动的温水中,经过相当长一段时间后.取袋内液体分别与碘水、含NaOH的Cu(OH)2(加热)反应,其现象分别是( )
| A. | 显蓝色,无明显现象 | B. | 显蓝色,出现红色沉淀 | ||
| C. | 无明显现象,无明显现象 | D. | 无明显现象,出现红色沉淀 |
7.下列说法不正确的是( )
| A. | 天然油脂没有固定的熔、沸点 | |
| B. | 米饭在嘴中越咀嚼越甜的原因是淀粉水解生成甜味物质 | |
| C. | 油脂、乙醇是人体必需的营养物质 | |
| D. | 水果因含有酯类物质而具有香味 |
17.短周期元素X、Y、Z、M、W的原子序数增大,X的气态氰化物能使湿润的红色石蕊试纸变蓝,X与W最外层电子数之和等于Y最外层电子数的2倍,在短周期主族元素中Z的原子半径最大,M的最外层电子数是电子层数的2倍,下列说法不正确的是( )
| A. | Y的气态氢化物比X的稳定 | |
| B. | 元素M存在多种同素异形体 | |
| C. | Z与Y形成的化合物只含有离子键 | |
| D. | W的最高价氧化物对应水化物的酸性比M的强 |
18.a、b、c、d是原子序数依次增大的主族元素,它们的最外层电子数分别为4、1、x、7,c原子的电子层数等于x,下列说法正确的是( )
| A. | 元素a与氢元素能形成多种原子个数之比为1:1的化合物 | |
| B. | 元素b的单质不能与无水乙醇反应 | |
| C. | 元素c与元素d形成的化合物的水溶液呈碱性 | |
| D. | 元素a与元素d形成的化合物中肯定含有极性键,不可能含有非极性键 |