题目内容
把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( )
A.(b-a)/V mol·L-1 B.(2b-a)/V mol·L-1
C.2(b-a)/V mol·L-1 D.2(2b-a)/V mol·L-1
D
【解析】由离子方程式:2OH-+Mg2+ =Mg(OH)2↓可知,OH-为a mol,则Mg2+为a/2 mol,MgSO4为a/2 mol;由离子方程式: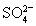 +Ba2+=BaSO4↓可知,Ba2+为b mol,
+Ba2+=BaSO4↓可知,Ba2+为b mol,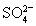 为b mol,MgSO4和K2SO4共b mol,则K2SO4为(b-a/2) mol,其含有的K+为(b-a/2) mol×2= (2b-a) mol;原混合溶液中的K+为2×(2b-a) mol;所以原混合溶液中钾离子的浓度为
为b mol,MgSO4和K2SO4共b mol,则K2SO4为(b-a/2) mol,其含有的K+为(b-a/2) mol×2= (2b-a) mol;原混合溶液中的K+为2×(2b-a) mol;所以原混合溶液中钾离子的浓度为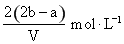 。
。
本题易错选B,其错误根源是只求出一份溶液中钾离子的物质的量,就直接除以总体积而得出答案。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案如图是某硫酸试剂瓶标签上的部分文字。据此,下列说法正确的是( )
硫酸 化学纯(CP)(500 mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84 g/cm3 质量分数:98% |
A.该硫酸的物质的量浓度为9.2 mol/L
B.1 mol Zn与足量的该硫酸反应生成2 g氢气
C.该硫酸与等体积水混合所得溶液的物质的量浓度等于9.2 mol/L
D.向50 mL该硫酸溶液中加入足量的铜片,加热充分反应后,被还原的硫酸的物质的量小于0.46 mol





