题目内容
12.下列物质中,属于含有极性键的离子晶体的是( )| A. | CH3COOH | B. | Na2O2 | C. | NaOH | D. | MgCl2 |
分析 活泼金属和活泼金属元素之间易形成离子键,同种非金属元素之间易形成非极性共价键,不同非金属元素之间易形成极性共价键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物,据此分析解答.
解答 解:A、CH3COOH是分子晶体,不是离子晶体,故A错误;
B、Na2O2是离子晶体,但其中含有的是离子键和非极性共价键,无极性共价键,故B错误;
C、NaOH是离子晶体,其中H和O原子间为极性共价键,故C正确;
D、MgCl2为离子晶体,结构中无共价键,故D错误.
故选C.
点评 本题考查化学键及化合物类型判断,为高频考点,明确物质构成微粒及微粒之间作用力即可解答,注意过氧化钠中存在的化学键及电子式书写方法,为易错点.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
3.下列物质的分子中既有σ键又有π键的是( )
①NH3 ②HClO ③O2 ④H2O2 ⑤HCHO(甲醛) ⑥C2H2.
①NH3 ②HClO ③O2 ④H2O2 ⑤HCHO(甲醛) ⑥C2H2.
| A. | ③⑤⑥ | B. | ③④⑤⑥ | C. | ①③⑥ | D. | ①②③ |
20.下列有关化学用语表示正确的是( )
| A. | 26Fe的原子结构示意图: | B. | 氮化硅的化学式:Si3N4 | ||
| C. | 基态氮原子的电子排布图: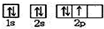 | D. | 29Cu的电子排布式:[Ar]3d94s2 |
7.下列离子方程式书写正确的是( )
| A. | 钠与水的反应 Na+H2O═OH-+H2↑ | |
| B. | NaHCO3溶液与盐酸的反应 CO32-+2H+═H2O+CO2↑ | |
| C. | 用FeCl3溶液腐蚀铜线路板 Cu+Fe3+═Cu2++Fe2+ | |
| D. | AlCl3溶液中加入过量氢氧化钠溶液 Al3++4OH-═AlO2-+2H2O |
17.下列说法正确的是( )
| A. | H2、SO2、CO均可用浓硫酸干燥 | |
| B. | 固态共价化合物不能导电,熔融态的共价化合物能导电 | |
| C. | SO2通入氯化钡溶液中生成白色沉淀 | |
| D. | 酸性氧化物一定是非金属氧化物,因此不能与酸溶液发生反应 |
4.下列化学用语的理解正确的是( )
| A. | 电子式: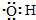 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 | |
| B. | 离子结构示意图: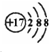 可以表示35Cl-,也可以表示37Cl- 可以表示35Cl-,也可以表示37Cl- | |
| C. | 比例模型: 可以表示甲烷分子,也可以表示四氯化碳分子 可以表示甲烷分子,也可以表示四氯化碳分子 | |
| D. | 聚丙烯的结构简式: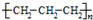 |
1.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 46g乙醇中含有的C-H键的数目为6NA | |
| B. | 0.lmol丙烯酸中含有的双键的数目为0.lNA | |
| C. | 1mol甲基(-CH3)中含有的电子总数为9NA | |
| D. | 标准状况下,22.4 L己烷完全燃烧生成的CO2分子的数目约为6NA |