题目内容
9. 某小组在研究前18号元素时发现:依据不同的标准和规律,元素周期表有不同的排列形式.如果将它们按原子序数递增的顺序排列,可形成图所示的“蜗牛”形状,图中每个“.”代表一种元素,其中P点代表氢元素.
某小组在研究前18号元素时发现:依据不同的标准和规律,元素周期表有不同的排列形式.如果将它们按原子序数递增的顺序排列,可形成图所示的“蜗牛”形状,图中每个“.”代表一种元素,其中P点代表氢元素.(1)X元素符号为Al.
(2)M与Z两种元素形成的化合物含有的化学键为离子键.
(3)下列说法正确的是d.
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L+>K2?
d.由K、L两种元素组成的化合物中可能含有共价键.
分析 (1)X元素是Al元素;
(2)M是Mg元素、Z是Cl元素,二者通过得失电子生成离子化合物氯化镁;
(3)a.K为O元素,Z为F元素,其氢化物分子间形成的氢键数目越多,沸点越高;
b.虚线相连的元素处于同一族;
c.电子层数越多其离子半径越大,电子层结构相同的离子,离子半径随着原子序数增大而减小;
d.由K、L两种元素组成的化合物可能是Na2O或Na2O2,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键;
解答 解:(1)X原子核外有3个电子层、最外层电子数是3,X元素是Al元素,故答案为:Al;
(2)M是Mg元素、Z是Cl元素,二者通过得失电子生成离子化合物氯化镁,其电子式为 含有离子键,故答案为:离子键;
含有离子键,故答案为:离子键;
(3)a.K为O元素,Z为F元素,水、氟化氢分子间均有氢键,但是水分子间形成的氢键数目多余HF分子间形成的氢键数目,其氢化物分子间形成的氢键数目越多,沸点越高,所以水的沸点大于氟化氢,故错误;
b.虚线相连的元素处于同一族,图中包含主族和零族元素,不全部是主族,故错误;
c.电子层数越多其离子半径越大,电子层结构相同的离子,离子半径随着原子序数增大而减小,所以离子半径从小到大顺序为X3+<L+<K2?,故错误;
d.由K、L两种元素组成的化合物可能是Na2O或Na2O2,过氧化钠中存在离子键和共价键,故正确;
故答案为:d.
点评 本题考查元素周期表和元素周期律综合应用,侧重考查学生分析问题、解答问题能力,涉及原子结构、元素周期律,综合性较强,难度中等.

练习册系列答案
相关题目
19.X、Y、Z、W是原子序数依次增大的短周期元素,其中X原子与Y原子可形成具有10个电子的M分子,Y元素最高价氧化物对应的水化物与M反应会生成一种离子化合物,Z元素原子的最外层电子数为2,W元素的单质可用于自来水的消毒杀菌.下列说法正确的是( )
| A. | 非金属性:Y>X>W | |
| B. | Z与W形成的化合物中存在共价键 | |
| C. | 一定条件下Z3Y2与水反应可生成M | |
| D. | 工业上用W单质与澄清石灰水反应制取漂白粉 |
1.(1)表是第三周期部分元素氧化物和氟化物的熔点和摩氏硬度:
①两种氧化物MgO和SiO2的晶体类型分别是离子晶体、原子晶体
②表格中几种氟化物熔点差异的主要原因是NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低;Mg2+的半径比Na+的半径小,Mg2+带2个单位正电荷数比Na+多,故MgF2的熔点比NaF高
③1mol SiO2中含有4molSi-O键,Si和O原子配位数之比为2:1
④NaF、MgF2、MgO、SiF4、SiO2中化学键能够代表分子真实组成的是SiF4.
(2)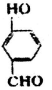 比
比 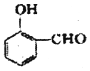 的沸点高(填“高”或“低”).
的沸点高(填“高”或“低”).
| 化合物 | NaF | MgF2 | MgO | SiF4 | SiO2 |
| 熔点/K | 1266 | 1534 | 3125 | 183 | 1983 |
| 摩氏硬度 | 3,2 | 6.0 | 6.5 | 7 |
②表格中几种氟化物熔点差异的主要原因是NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低;Mg2+的半径比Na+的半径小,Mg2+带2个单位正电荷数比Na+多,故MgF2的熔点比NaF高
③1mol SiO2中含有4molSi-O键,Si和O原子配位数之比为2:1
④NaF、MgF2、MgO、SiF4、SiO2中化学键能够代表分子真实组成的是SiF4.
(2)
 比
比  的沸点高(填“高”或“低”).
的沸点高(填“高”或“低”).
9.工业上根据污水中所含物质或离子的不同,有多种处理方法:
请回答下列问题:
(1)在中和法中,若用CO2来除去污水中的某种离子,其离子方程式为OH-+CO2=HCO3-;
(2)在氧化还原法中,常用Cl2氧化污水中有毒的CN-,使其转化为CO2和N2,若参加反应的Cl2与CN-的物质的量之比为5:2,则该反应的离子方程式为5Cl2+2CN-+4H2O═10Cl-+2CO2+N2+8H+;
(3)已知有关物质的Ksp如下表:
如图为化学沉淀法处理污水的工艺流程示意图.
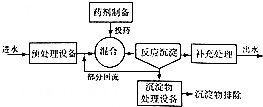
①在沉淀法中,NaOH与Na2S相比,除去污水中的Cu2+效果较好的是Na2S;
②若某污水中能与上述沉淀剂反应的阳离子只有Hg2+,且含量为400mg/L,则处理10L这样的污水至少需要加入该沉淀剂1.6g(精确到0.1).
| 污水中所含离子 | H+、OH- | CN- | Cu2+、Hg2+ |
| 处理方法 | 中和法 | 氧化还原法 | 沉淀法 |
(1)在中和法中,若用CO2来除去污水中的某种离子,其离子方程式为OH-+CO2=HCO3-;
(2)在氧化还原法中,常用Cl2氧化污水中有毒的CN-,使其转化为CO2和N2,若参加反应的Cl2与CN-的物质的量之比为5:2,则该反应的离子方程式为5Cl2+2CN-+4H2O═10Cl-+2CO2+N2+8H+;
(3)已知有关物质的Ksp如下表:
| 物质 | Cu(OH)2 | CuS | FeS | PbS | HgS | CdS |
| Ksp | 2.2×10-20 | 8.5×10 -45 | 6.3×10 -18 | 3.4×10-28 | 4×10-53 | 8×10-29 |

①在沉淀法中,NaOH与Na2S相比,除去污水中的Cu2+效果较好的是Na2S;
②若某污水中能与上述沉淀剂反应的阳离子只有Hg2+,且含量为400mg/L,则处理10L这样的污水至少需要加入该沉淀剂1.6g(精确到0.1).
 已知A、B、C、D、E都是周期表中前四周期的元素,它们的原子序数依次增大.其中A元素原子的核外p电子数比s电子数少1.C是电负性最大的元素.D原子次外层电子数是最外层电子数2倍,E是第Ⅷ族中原子序数最小的元素.
已知A、B、C、D、E都是周期表中前四周期的元素,它们的原子序数依次增大.其中A元素原子的核外p电子数比s电子数少1.C是电负性最大的元素.D原子次外层电子数是最外层电子数2倍,E是第Ⅷ族中原子序数最小的元素.