题目内容
下列说法或表达正确的是( )
①活性炭、SO2和HClO都具有漂白作用,且漂白的化学原理相同
②向100 mL0.1 mol/L 的溴化亚铁溶液中通入0.05 mol的氯气时发生反应的离子方程式:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
③斜长石KAlSi3O8的氧化物形式可表示为:K2O?Al2O3?3SiO2
④酸性条件下KIO3溶液与KI溶液发生反应生成I2时的离子方程式:
IO3-+5I-+3H2O=I2+6OH-
⑤碳酸氢根离子的电离方程式可表示为:
⑥元素周期表中,从上到下,卤族元素的非金属性逐渐减弱,氢卤酸的酸性依次减弱
⑦500℃、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)  2NH3(g) △H= 38.6 kJ·mol-1
2NH3(g) △H= 38.6 kJ·mol-1
A.全部 B.②⑤ C.②③④⑦ D.②④⑦
B
【解析】
试题解析:①活性炭、SO2和HClO的漂白原理不同,活性炭属于吸附型漂白,二氧化硫属于结合型漂白,次氯酸属于氧化性漂白,故①错误;③斜长石KAlSi3O8的写成氧化物形式为:K2O?Al2O3?6SiO2,要保证各元素的原子个数比不变,故③错误;④酸性条件下不能生成氢氧根离子,故④错误;⑥从上到下,卤族元素的非金属性逐渐减弱,气态氢化物的稳定性减弱,其水溶液中氢卤酸的酸性依次增强,故⑥错误;⑦工业合成氨的反应为放热反应,△H为负值,故⑦错误;故选B.

 通城学典默写能手系列答案
通城学典默写能手系列答案(18分)C、O、Na、Al、S、Cl是常见的六种元素
(1)C元素位于元素周期表第 周期,第 族;C元素的一种同位素可以测定文物年代,这种同位素的符号为
(2)用“大于”“小于”或“等于”填空
离子半径 | 还原性 | 得电子能力 |
N3- Al3+ | O2- S2- | 35Cl 37Cl |
(3)① CaCO3和适量HCl溶液反应时,每产生4.4 g 气体(不考虑气体溶解),放热a kJ,则该反应的热化学方程式为 。
②上述反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得pH变化曲线如图所示


请用离子方程式表示B-C段发生的反应:
(4)氢气、氧气常用来作燃料电池,写出电解质为氢氧化钠溶液时负极上的电极方程式
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
阳离子 | Ag+、Na+ |
阴离子 | NO3—、SO42—、Cl- |
下图Ⅰ所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了27 g。常温下各烧杯中溶液的pH与电解时间t的关系如下图Ⅱ所示。据此回答下列问题:
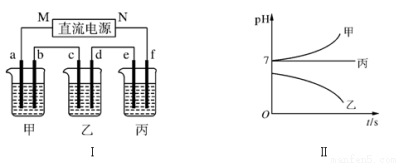
(1)M为电源的________(填“正”或“负”)极,A是________(填写化学式)。
(2)计算电极f上生成的气体在标准状况下的体积:________。
(3)写出乙烧杯的电解池反应:________________________________________________。
(4)要使丙恢复到原来的状态,应加入________ g ________(填写化学式)。