题目内容
19.能将直馏汽油、裂化汽油、乙醇、四氯化碳四种液体鉴别出来的试剂是( )| A. | 水 | B. | AgNO3溶液 | C. | 高锰酸钾 | D. | 溴水 |
分析 四氯化碳不溶于水,密度比水大,酒精和水混溶,裂化汽油中含不饱和烃可与溴水发生加成反应而褪色,直馏汽油与溴水萃取分层,可用溴水鉴别有机物.
解答 解:A.水不能鉴别直馏汽油、裂化汽油,故A不选;
B.均与硝酸银不反应,不能鉴别直馏汽油、裂化汽油,故B不选;
C.高锰酸钾不能鉴别裂化汽油、乙醇,均褪色,故C不选;
D.直馏汽油:色层在上,水在下;裂化汽油:能使溴水褪色最终得到分层的2层无色液体;乙醇与溴水互溶;四氯化碳:水层在上,色层在下,现象不同可鉴别,故D选;
故选D.
点评 本题考查有机物的鉴别,为高频考点,注意把握有机物性质的异同,根据物质的性质选择鉴别试剂,综合考查有机反应及萃取等,题目难度不大.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
9.下列有关有机化合物的说法正确的是( )
| A. | 用水可以区分苯和CCl4 | |
| B. | 有机物分子中都存在碳碳单键 | |
| C. | 做银镜反应实验后的试管内壁附有银,可用稀盐酸清洗 | |
| D. | 检验乙醇消去后的产物乙烯,可将气体直接通入酸性高锰酸钾溶液中 |
10.一定条件下,对于可逆反应X(g)+3Y(g)?2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1mol/L、0.3mol/L、0.08mol/L,则下列判断正确的是( )
| A. | c1:c2=3:1 | |
| B. | 平衡时,Y和Z的生成速率之比为2:3 | |
| C. | X、Y的转化率相等 | |
| D. | c1的取值范围为0 mol/L≤c1≤0.14 mol/L |
7.X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质.已知:甲+乙=丁+己,甲+丙=戊+己; 丁溶液为短周期元素中最高价氧化物对应水化物中碱性最强的物质.下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X | |
| B. | Y元素在周期表中的位置为第三周期第ⅣA族 | |
| C. | 1mol甲与足量的乙完全反应共转移了1mol电子 | |
| D. | 甲、乙、丙、丁、戊、己中含有的共价键的物质只有乙、丙、己 |
14.下列叙述正确的是( )
| A. | 铝粉与氧化镁共热可制取金属镁 | |
| B. | 铝分别与足量的 HCl溶液、足量的NaOH的溶液反应,产生的氢气前者多 | |
| C. | 可用Na2SiO3溶液和CO2反应来制备H2SiO3 | |
| D. | NaOH溶液可以盛装在带玻璃塞的磨口试剂瓶中 |
4.下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).
(1)下列化合物与氯化氢加成时,取代基对速率的影响与表中规律类似,其中反应速率最快的是A(填序号).
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH2CH3
C.CH2=CH CH3 D.CH2=CHCl
(2)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3+HBr→CH3CHBrCH3+CH3CH2Br
(主要产物)(次要产物)
请写出 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式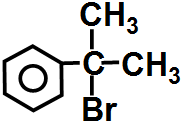 .
.
| 烯类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH2CH3
C.CH2=CH CH3 D.CH2=CHCl
(2)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3+HBr→CH3CHBrCH3+CH3CH2Br
(主要产物)(次要产物)
请写出
 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式 .
.
8.某有机物M的结构简式如图所示: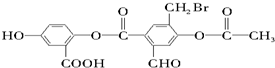 下列说法正确的是( )
下列说法正确的是( )
 下列说法正确的是( )
下列说法正确的是( )| A. | 1 mol M最多能与10×22.4 L氢气(标准状况)发生加成反应 | |
| B. | 1 mol M最多能与2 mol Na HCO3反应 | |
| C. | 1 mol M最多能与5 mol NaOH反应 | |
| D. | 1 mol M最多能与2 mol Na反应 |
1.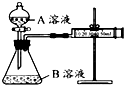 某实验小组利用 KMnO4 酸性溶液与弱酸 H2C2O4溶液反应进行“外界因素对反应速率 影响”的探究,设计实验方案如下:
某实验小组利用 KMnO4 酸性溶液与弱酸 H2C2O4溶液反应进行“外界因素对反应速率 影响”的探究,设计实验方案如下:
甲组:通过测定生成 CO2气体体积的方法来比较化学反应速率的大小.实验装置如图,实验时分 液漏斗中A溶液一次性放入B溶液中.
(注:实验中所用 KMnO4溶液均已加入相同量 H2SO4)
(1)写出锥形瓶中加入A溶液后发生反应的离子方程式:2MnO4-+5H2C2O4+6H+=2Mn2++l0CO2↑+8H2O.
(2)该组的实验目的是探究H2C2O4溶液浓度对化学反应速率的影响. 分析所给实验仪器,实现该实验目的还欠缺的仪器:秒表.
乙组:通过测定溶液褪色时间来判断反应速率快慢,实验记录如下表(各实验均在室温下进行):
(3)若实验①②是探究温度对化学反应速率影响,V1=30.0mL;设计实验④⑤的目的是探究产物是否对反应有催化作用.
(4)根据乙组的实验记录,下列结论正确的是C A.实验③中,V3=10
B.实验①③说明反应速率只与 KMnO4 浓度有关
C.根据实验①⑤可推出实验①中的反应速率变化是:起初较小,后明显变大,又逐渐变小.
 某实验小组利用 KMnO4 酸性溶液与弱酸 H2C2O4溶液反应进行“外界因素对反应速率 影响”的探究,设计实验方案如下:
某实验小组利用 KMnO4 酸性溶液与弱酸 H2C2O4溶液反应进行“外界因素对反应速率 影响”的探究,设计实验方案如下:甲组:通过测定生成 CO2气体体积的方法来比较化学反应速率的大小.实验装置如图,实验时分 液漏斗中A溶液一次性放入B溶液中.
| 序号 | A溶液 | B溶液 |
| ① | 2mL 0.2mol/L-1 H2C2O4溶液 | 4mL 0.01mol/L-1 KMnO4溶液 |
| ② | 2mL 0.1mol/L -1H2C2O4溶液 | 4mL 0.01mol/L-1 KMnO4溶液 |
(1)写出锥形瓶中加入A溶液后发生反应的离子方程式:2MnO4-+5H2C2O4+6H+=2Mn2++l0CO2↑+8H2O.
(2)该组的实验目的是探究H2C2O4溶液浓度对化学反应速率的影响. 分析所给实验仪器,实现该实验目的还欠缺的仪器:秒表.
乙组:通过测定溶液褪色时间来判断反应速率快慢,实验记录如下表(各实验均在室温下进行):
| 实验 编号 | 温度/℃ | 烧杯中所加的试剂及其用量 (mL) | 加入 少量固体 | 溶液褪色 时间(s) | |||
| 0.6mol•L-1 H2C2O4溶液 | H O | 0.2mol•L-1 KMnO4溶液 | 3mol•L-1 稀硫酸 | ||||
| ① | 25 | 30.0 | 20.0 | 30.0 | 20.0 | 无 | 1.8 |
| ② | 50 | V1 | V2 | 30.0 | 20.0 | 无 | 1.0 |
| ③ | 25 | 15.0 | V3 | 15.0 | 10.0 | 无 | 3.6 |
| ④ | 25 | 30.0 | 20.0 | 30.0 | 20.0 | K2SO4 | 1.8 |
| ⑤ | 25 | 30.0 | 20.0 | 30.0 | 20.0 | MnSO4 | 0.6 |
(4)根据乙组的实验记录,下列结论正确的是C A.实验③中,V3=10
B.实验①③说明反应速率只与 KMnO4 浓度有关
C.根据实验①⑤可推出实验①中的反应速率变化是:起初较小,后明显变大,又逐渐变小.
 .
.