题目内容
化学平衡常数K的应用具有现实意义,试完成以下填空:
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示 ,K值大小与温度的关系是:温度升高,K值 .(填一定增大、一定减小、或可能增大也可能减小).
(2)在密闭容器中,将2.0mol CO与10mol H2O混合加热到800℃,达到下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g) K=1.0,则CO的转化率为 .在800℃,若上述反应体系中各物质的浓度分别为c(CO)=2.0mol?L-1,c(H2O)=6.0mol?L-1,c(CO2)=3.0mol?L-1,c(H2)=4.5mol?L-1,则此时该反应向 方向移动.
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示
(2)在密闭容器中,将2.0mol CO与10mol H2O混合加热到800℃,达到下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g) K=1.0,则CO的转化率为
考点:化学平衡的影响因素
专题:化学平衡专题
分析:(1)化学平衡常数K=
,根据K与反应物浓度幂之积和生成物浓度幂之积之间的关系进性回答;
(2)令平衡时参加反应的CO的物质的量为xmol,根据三段式用x表示出平衡时各组分的物质的量,由于反应前后气体的物质的量不变,故利用物质的量代替浓度代入平衡常数列放出计算x的值,再根据转化率定义计算CO的转化率;
计算此时的浓度商Qc,与平衡常数相比判断反应进行方向,若Qc=k,则反应处于平衡状态,若Qc>K,则反应向逆反应进行,若Qc<K,反应向正反应进行.
| 生成物的浓度幂之积 |
| 反应物的浓度幂之积 |
(2)令平衡时参加反应的CO的物质的量为xmol,根据三段式用x表示出平衡时各组分的物质的量,由于反应前后气体的物质的量不变,故利用物质的量代替浓度代入平衡常数列放出计算x的值,再根据转化率定义计算CO的转化率;
计算此时的浓度商Qc,与平衡常数相比判断反应进行方向,若Qc=k,则反应处于平衡状态,若Qc>K,则反应向逆反应进行,若Qc<K,反应向正反应进行.
解答:
解:(1)平衡常数为生成物的浓度幂之积除以反应物的浓度幂之积,K越大,说明生成物越多,反应物越少,所以可逆反应进行的程度越大;当反应放热时,升高温度平衡向逆反应方向移动,当反应吸热时,升高温度平衡向正反应方向移动,温度升高,K可能增大,也可能减小,
故答案为:可逆反应进行的程度越大;可能增大也可能减小.
(2)令平衡时参加反应的CO的物质的量为xmol,则:
CO(g)+H2O(g)?CO2(g)+H2(g)
开始(mol):2 10 0 0
变化(mol):x x x x
平衡(mol):2-x 10-x x x
所以
=1,解得x=
mol
故CO的转化率为
×100%=83.3%;
在800℃,若上述反应体系中各物质的浓度分别为c(CO)=2.0mol?L-1,c(H2O)=6.0mol?L-1,c(CO2)=3.0mol?L-1,c(H2)=4.5mol?L-1,此时浓度商Qc=
=1.125>1,故反应向逆反应进行,
故答案为:83.3%;逆反应.
故答案为:可逆反应进行的程度越大;可能增大也可能减小.
(2)令平衡时参加反应的CO的物质的量为xmol,则:
CO(g)+H2O(g)?CO2(g)+H2(g)
开始(mol):2 10 0 0
变化(mol):x x x x
平衡(mol):2-x 10-x x x
所以
| x×x |
| (2-x)(10-x) |
| 5 |
| 3 |
故CO的转化率为
| ||
| 2mol |
在800℃,若上述反应体系中各物质的浓度分别为c(CO)=2.0mol?L-1,c(H2O)=6.0mol?L-1,c(CO2)=3.0mol?L-1,c(H2)=4.5mol?L-1,此时浓度商Qc=
| 3×4.5 |
| 2×6 |
故答案为:83.3%;逆反应.
点评:本题考查化学平衡常数的有关计算,难度中等,注意平衡常数的用途:1、判断反应进行的程度,2、判断反应的热效应,3、判断反应进行的方向,4、计算转化率等.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目

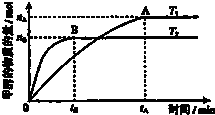 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.请回答下列问题: