题目内容
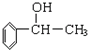 (1)苏合香醇可以用作食用香精,其结构简式如图所示.
(1)苏合香醇可以用作食用香精,其结构简式如图所示.苏合香醇的分子式为
①取代反应 ②加成反应 ③氧化反应 ④加聚反应
苏合香醇属于酚类有机物的同分异构体共有
(2)
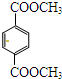 的同分异构体有多种,满足下列条件的共有
的同分异构体有多种,满足下列条件的共有①苯环上只有两个取代基
②1mol 与足量的NaHCO3溶液反应生成2mol CO2气体.
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:(1)苏合香醇为C6H5CH(OH)CH3,由-OH和苯环分析其性质;属于酚,含酚-OH,则2个C可为2个甲基或1个乙基;
(2) 的同分异构体有多种,满足①苯环上只有两个取代基,②1mol 与足量的NaHCO3溶液反应生成2mol CO2气体,则含2个-COOH,2个取代基分别为-COOH、CH2CH2COOH,或-COOH、-CH(CH3)COOH,或-CH2COOH、-CH2COOH,或-CH3、-CH(COOH)2,均存在邻、间、对三种位置.
的同分异构体有多种,满足①苯环上只有两个取代基,②1mol 与足量的NaHCO3溶液反应生成2mol CO2气体,则含2个-COOH,2个取代基分别为-COOH、CH2CH2COOH,或-COOH、-CH(CH3)COOH,或-CH2COOH、-CH2COOH,或-CH3、-CH(COOH)2,均存在邻、间、对三种位置.
(2)
 的同分异构体有多种,满足①苯环上只有两个取代基,②1mol 与足量的NaHCO3溶液反应生成2mol CO2气体,则含2个-COOH,2个取代基分别为-COOH、CH2CH2COOH,或-COOH、-CH(CH3)COOH,或-CH2COOH、-CH2COOH,或-CH3、-CH(COOH)2,均存在邻、间、对三种位置.
的同分异构体有多种,满足①苯环上只有两个取代基,②1mol 与足量的NaHCO3溶液反应生成2mol CO2气体,则含2个-COOH,2个取代基分别为-COOH、CH2CH2COOH,或-COOH、-CH(CH3)COOH,或-CH2COOH、-CH2COOH,或-CH3、-CH(COOH)2,均存在邻、间、对三种位置.解答:
解:(1)苏合香醇为C6H5CH(OH)CH3,分子式为C8H10O,由-OH可知能发生取代、氧化反应,含苯环可发生加成反应,而不能发生加聚反应;属于酚,含酚-OH,则2个C可为2个甲基或1个乙基,若为-OH、CH2CH3,存在邻、间、对3种,对甲基苯酚一种,邻甲基苯酚2种,间甲基苯酚3种,共9种,
故答案为:C8H10O;④;9;
(2) 的同分异构体有多种,满足①苯环上只有两个取代基,②1mol 与足量的NaHCO3溶液反应生成2mol CO2气体,则含2个-COOH,2个取代基分别为-COOH、CH2CH2COOH,或-COOH、-CH(CH3)COOH,或-CH2COOH、-CH2COOH,或-CH3、-CH(COOH)2,均存在邻、间、对三种位置,则同分异构体的数目为4×3=12种,
的同分异构体有多种,满足①苯环上只有两个取代基,②1mol 与足量的NaHCO3溶液反应生成2mol CO2气体,则含2个-COOH,2个取代基分别为-COOH、CH2CH2COOH,或-COOH、-CH(CH3)COOH,或-CH2COOH、-CH2COOH,或-CH3、-CH(COOH)2,均存在邻、间、对三种位置,则同分异构体的数目为4×3=12种,
故答案为:12.
故答案为:C8H10O;④;9;
(2)
 的同分异构体有多种,满足①苯环上只有两个取代基,②1mol 与足量的NaHCO3溶液反应生成2mol CO2气体,则含2个-COOH,2个取代基分别为-COOH、CH2CH2COOH,或-COOH、-CH(CH3)COOH,或-CH2COOH、-CH2COOH,或-CH3、-CH(COOH)2,均存在邻、间、对三种位置,则同分异构体的数目为4×3=12种,
的同分异构体有多种,满足①苯环上只有两个取代基,②1mol 与足量的NaHCO3溶液反应生成2mol CO2气体,则含2个-COOH,2个取代基分别为-COOH、CH2CH2COOH,或-COOH、-CH(CH3)COOH,或-CH2COOH、-CH2COOH,或-CH3、-CH(COOH)2,均存在邻、间、对三种位置,则同分异构体的数目为4×3=12种,故答案为:12.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重同分异构体推断的考查,注意酚、羧酸的性质,题目难度不大.

练习册系列答案
相关题目
设NA为阿佛加德罗常数,则下列叙述正确的是( )
| A、常温常压下,48gO3气体含有NA个O3分子 |
| B、标准状况下,含4molHCl的浓盐酸与足量MnO2反应可生成22.4LCl2 |
| C、1L0.5mol?L-1Na2CO3溶液中含有0.5NA个CO32- |
| D、标准状况下,33.6LH2O含有1.5NA个H2O分子 |
化学与生产、生活、社会密切相关.下列说法中不正确的是( )
| A、不需要通过化学反应就能从海水中获得食盐和淡水 |
| B、铁在潮湿的空气中放置,易发生化学腐蚀而生锈 |
| C、高空臭氧层吸收太阳紫外线,保护地球生物;低空过量臭氧是污染气体,对人体有害 |
| D、氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
短周期元素A、B、C、D的原子序数依次增大,它们的原子序数之和为36,且原子最外层电子数之和为14;A、C原子的最外层电子数之和等于B原子的次外层电子;A与C,B与D均为同主族元素.下列叙述正确的是( )
| A、B元素组成的一种单质具有漂白性,能使KMnO4溶液紫色褪去 |
| B、B、D两种元素形成的一种化合物也具有一定的漂白性,能使紫色石蕊紫色褪去 |
| C、C元素分别与A元素和B元素形成的化合物都是离子晶体,一定均与水反应生成强碱和无色气体 |
| D、A2B的热稳定性强于A2D、沸点也高于A2D,但解释的理由不相同 |
下列是四位同学对“化学与健康”这一话题发表的见解,其中正确的是( )
| A、维生素在天然食品中含量丰富,所以加工后的食品中维生素含量也高 |
| B、人体细胞中的酸碱平衡是不能通过选择食物调节的 |
| C、为了食品安全,我国应该禁止使用食品防腐剂 |
| D、食用植物油的主要成分是高级脂肪酸甘油酯,是人体所需营养物质 |
 铈、铬、钴、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用.
铈、铬、钴、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用.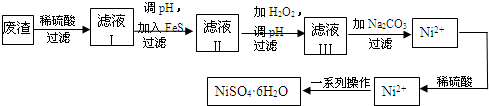
 有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示.电池正极的电极反应式是
有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示.电池正极的电极反应式是