题目内容
设NA代表阿伏加德罗常数,下列叙述正确的是( )
| A、0.1 mol/L NaHCO3和0.1 mol/L Na2CO3混合溶液1L,HCO3-,CO32-的总数为0.2NA |
| B、向密闭容器中充入2molN2和3molH2,在一定条件下发生反应,达到平衡时,混合气体中NH3的体积分数为23.45%,则H2和NH3所含的H原子总数为6NA |
| C、若1L0.1 mol/L的CH3COOH溶液含CH3COO- 数为aNA,则1L0.3 mol/L的CH3COOH溶液含CH3COO- 数小于0.3aNA |
| D、反应N2+3H2?2NH3达平衡时,每形成6NA个N-H键,也生成14克N2 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、HCO3-、CO32-发生水解可生成碳酸;
B、氨气中的H来源于H2,根据氢原子守恒计算;
C、CH3COOH溶液浓度越大,水解程度越小;
D、根据达到化学平衡时,正逆反应速率相等计算.
B、氨气中的H来源于H2,根据氢原子守恒计算;
C、CH3COOH溶液浓度越大,水解程度越小;
D、根据达到化学平衡时,正逆反应速率相等计算.
解答:
解:A、HCO3-、CO32-发生水解可生成碳酸,导致溶液中HCO3-,CO32-的总数小于0.2NA,故A错误;
B、氨气中的H来源于H2,H2和NH3所含的H原子总数即为3molH2中所含H原子数,3molH2中所含H原子数为3mol×2×NA mol-1=6NA,故B正确;
C、CH3COOH溶液浓度越大,水解程度越小,若1L0.1 mol/L的CH3COOH溶液含CH3COO- 数为aNA,则1L0.3 mol/L的CH3COOH溶液含CH3COO- 数大于0.3aNA,故C错误;
D、形成6NA个N-H键,说明生成2mol氨气,化学平衡时正逆反应速率相等,生成1mol氮气,即为生成14g氮气,故D正确;
故选BD.
B、氨气中的H来源于H2,H2和NH3所含的H原子总数即为3molH2中所含H原子数,3molH2中所含H原子数为3mol×2×NA mol-1=6NA,故B正确;
C、CH3COOH溶液浓度越大,水解程度越小,若1L0.1 mol/L的CH3COOH溶液含CH3COO- 数为aNA,则1L0.3 mol/L的CH3COOH溶液含CH3COO- 数大于0.3aNA,故C错误;
D、形成6NA个N-H键,说明生成2mol氨气,化学平衡时正逆反应速率相等,生成1mol氮气,即为生成14g氮气,故D正确;
故选BD.
点评:本题考查了阿伏伽德罗常数,为高考高频考点,侧重于盐类的水解、守恒思想、化学平衡判定等核心知识的分析和应用,题目综合性较强,难度一般.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、利用丁达尔现象可以鉴别胶体和溶液 |
| B、在豆浆里加入盐卤做豆腐与胶体的聚沉有关 |
| C、胶体与溶液的分离可用渗析的方法 |
| D、KCl溶液、淀粉溶液和纯水都属于分散系 |
 下列有关实验没有明显错误的是( )
下列有关实验没有明显错误的是( )| A、使用湿润过的pH试纸测量某溶液的pH |
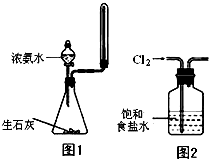
| B、实验室可以用图1所示装置来制取少量氨气 |
| C、用量筒量取20 mL 0.50mol?L-1H2SO4溶液于烧杯中,加水80 mL,配制成0.10mol?L-1H2SO4溶液 |
| D、实验室用图2所示装置除去Cl2中的少量HCl |
下列说法正确的是( )
| A、绿色化学就是研究绿色物质的化学 |
| B、烷烃是一类饱和链烃,其分子都是直线型的 |
| C、甲烷是烷烃中碳元素的质量分数最低的,也是最简单的烃 |
| D、“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是指纤维素和油脂 |
下列关于卤素及其化合物的叙述正确的是( )
| A、HF水溶液可存放在玻璃试剂瓶中 |
| B、Br2可从KCl溶液中置换出氯 |
| C、F、Cl、Br、I的非金属性依次减弱 |
| D、HF、HCl、HBr、HI的稳定性依次增强 |
下列说法中,不正确的是( )
| A、大多数有机物难溶于水,易溶于汽油、苯等有机溶剂 |
| B、有机物的熔点低 |
| C、有机物都是非电解质,不易导电 |
| D、有机物的化学反应比较复杂,一般较慢,且常伴有副反应发生 |
下列说法正确的是( )
| A、pH=6.8的溶液一定显酸性 |
| B、电离平衡常数(K)只与弱电解质本身有关,与其它外部因素无关 |
| C、0.1 mol?L-1的硫化钠溶液中:c(H+)+c(Na+)=c(OH-)+c(HS-)+c(S2-) |
| D、相同物质的量浓度的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,则c(NH4+)由大到小的顺序是:①>②>③ |
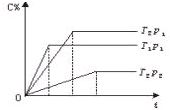 可逆反应:2A(g)+B(g)?2C(g)在温度分别为T1、T2,压强分别为p1、p2条件下测得C的体积分数与时间t的关系如图所示,下列判断正确的是:
可逆反应:2A(g)+B(g)?2C(g)在温度分别为T1、T2,压强分别为p1、p2条件下测得C的体积分数与时间t的关系如图所示,下列判断正确的是:( )
| A、p2<p1,逆反应放热 |
| B、p2>p1,正反应放热 |
| C、p2>p1,正反应吸热 |
| D、p2<p1,逆反应吸热 |