题目内容
在25°C下,将,amol·L-1的醋酸(HAc)与0.01mol·L-1的氢氧化钠溶液等体积混合,反应平衡时溶液中c(Na+)=c(Ac-)。则下列说法中,不正确的是 ( )
A.此时醋酸和氢氧化钠溶液恰好中和
B.反应后混合液的导电性一定弱于0.01mol·L-1的氢氧化钠溶液
C.溶液中的离子浓度大小的顺序为c(Na+)=c(Ac-)>c(OH-)= c(H+)
D.a肯定大于0.01
A解析:A项,由反应平衡时溶液中c(Na+)=c(Ac-),推出n(HAc)>n(NaOH),故说成恰好酸碱恰好中和是错误的;由溶液中的电荷守恒可知,c(Na+)=c(Ac-),则c(H+)=c(OH-),故B、C正确; D项,当醋酸溶液的浓度为0.01mol·L-1时,溶液呈碱性,现呈中性,则a肯定大于0.01,D正确。

练习册系列答案
相关题目


 (1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g) 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g) 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题: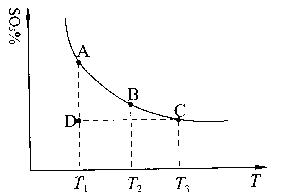

 (填“>”、“<”或“=”)
(填“>”、“<”或“=”) )
) 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:

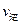 (填“>”、“<”或“=”)
(填“>”、“<”或“=”) )
) 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
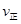
 (填“>”、“<”或“=”)(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(填“>”、“<”或“=”)(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
 )
)