题目内容
8.室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是( )| A. | 溶液中导电粒子的数目增加,导电性增强 | |
| B. | 醋酸的电离程度增大,[H+]减小 | |
| C. | 电离平衡向右移动,电离常数Ka减少 | |
| D. | 稀释后溶液中由水电离出的[H+]=1×10-11 mol/L |
分析 A.加水稀释促进醋酸电离,但氢离子和醋酸根离子浓度减小;
B.加水稀释促进醋酸电离,但氢离子浓度减小;
C.电离常数Ka,是温度的函数;
D.稀释后溶液的pH未知,无法计算水电离出氢离子浓度.
解答 解:A.加水稀释促进醋酸电离,但氢离子和醋酸根离子浓度减小,溶液导电能力与离子浓度成正比,所以溶液导电性减弱,故A错误;
B.加水稀释促进醋酸电离,溶液中氢离子个数增大程度小于溶液体积增大程度,所以氢离子浓度减小,故B正确;
C.电离常数Ka,是温度的函数,温度不变电离平衡常数不变,故C错误;
D.稀释后溶液的pH未知,虽然水的离子积常数不变,但无法计算水电离出氢离子浓度,故D错误;
故选B.
点评 本题考查了弱电解质的电离,明确弱电解质电离特点是解本题关键,加水稀释促进醋酸电离,但氢离子浓度降低,很多同学往往认为“促进电离,氢离子浓度增大”而导致错误,为易错点.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
18.下列各溶液中,微粒的物质的量浓度关系不正确的是( )
| A. | 常温下,将pH=2的盐酸和pH=12的氨水等体积混合后:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| B. | 0.1 mol•L-1 Na2CO3溶液:2c(Na+)=c(HCO3-)+c(CO32?)+c(H2CO3) | |
| C. | 0.1 mol•L-1 NH4Cl溶液:c(NH4+)=c( Cl-) | |
| D. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
3.下列有关盐类水解的说法中,正确的是( )
| A. | 所有的盐在水溶液中都能水解 | |
| B. | 盐类水解一定都显酸性或碱性 | |
| C. | 盐类的水解反应是酸碱中和反应的逆反应,因此盐类水解是吸热反应 | |
| D. | 盐类水解抑制了水的电离 |
17.海水是一个巨大的化学资源库,有关海水综合利用的说法正确的是( )
| A. | 海水中含有钾元素,只需经过物理变化就可以得到钾单质 | |
| B. | 海水蒸发制海盐的过程中发生了化学变化 | |
| C. | 利用潮汐发电是将化学能转化为电能 | |
| D. | 从海水中可以得到NaCl,电解熔融NaCl可制备金属钠 |
18.等量的铁分别与足量的盐酸、水蒸气在一定的条件下充分反应,则在相同的条件下,产生氢气的体积比是( )
| A. | 1:1 | B. | 2:3 | C. | 3:4 | D. | 4:3 |
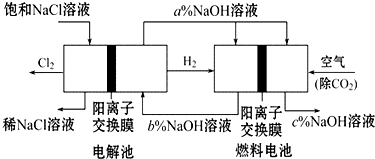 有一种节能的氯碱工业新工艺,将电解池与燃料电池相结合,相关流程如图(电极未标出).回答下列有关问题:
有一种节能的氯碱工业新工艺,将电解池与燃料电池相结合,相关流程如图(电极未标出).回答下列有关问题: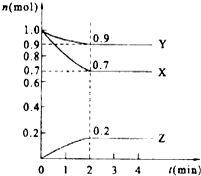 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.