题目内容
13.在自然界中不存在游离态的元素是( )| A. | 碳 | B. | 硫 | C. | 铁 | D. | 铝 |
分析 元素存在状态由以单质形式存在的为游离态,以化合物形式存在的为化合态,根据元素的活泼性来判断元素在自然界的存在形式,钠、氯、镁性质活泼是以化合态存在,镁主要以化合态存在于海水中,硫以游离态存在.
解答 解:A.碳是不活泼非金属元素,自然界中有游离态碳,如煤炭,故A错误;
B.硫元素在自然界中火山口附近有游离态的硫元素存在,故B错误;
C.铁是活泼金属,易失电子自然界中无游离态,陨石中含游离态的铁,故C错误;
D.因铝最外层电子少,易失去,易被还原,从而性质活泼,只能以化合态存在,故D正确;
故选D.
点评 本题主要考查了元素在自然界的存在形式,注意元素单质的活泼性分析,游离态是单质形式存在,化合态是以化合态存在,题目较简单.

练习册系列答案
相关题目
3.下列判断错误的是( )
| A. | 沸点:NH3>PH3>AsH3 | B. | 熔点:Si3N4>NaCl>Sil4 | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
4.下列各溶液中一定能大量共存的离子组是( )
| A. | 常温下,c(H+)=10-13mol•L-1的溶液中:Na+、AlO2-、S2-、SO32- | |
| B. | 使pH试纸呈红色的溶液中:Fe2+、I-、NO3-、Cl- | |
| C. | 加入铝粉有氢气生成的溶液中:Mg2+、Cu2+、SO42-、K+ | |
| D. | 常温下,由水电离出的c(H+)•c(OH-)=1.0×10-26的溶液中:K+、Na+、HCO3-、Ca2+ |
1.下列说法不正确的是( )
| A. | 化学键的断裂与形成一定伴随着电子的转移和能量变化 | |
| B. | 碘晶体是分子晶体,加热升华过程中只需克服分子间作用力 | |
| C. | 二氧化硅晶体属于原子晶体,每个Si通过共价键与4个O结合 | |
| D. | 氯化钠的电离是一个破坏离子键的过程 |
8.下列叙述正确的是( )
| A. | NH4+、Al3+、Cl-、HCO3-在溶液中能大量共存 | |
| B. | H2O2的电子式是: | |
| C. | AlCl3溶液中加入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 铁锈是化合物,可用Fe2O3•nH2O(2<n<3)表示 |
18.如图所示分离混合物时常用的仪器,从左至右,对应的混合物分离操作方法正确的是( )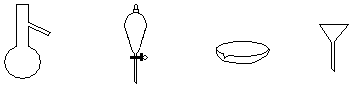

| A. | 蒸发、过滤、蒸馏、分液 | B. | 蒸馏、分液、蒸发、过滤 | ||
| C. | 蒸馏、过滤、蒸发、分液 | D. | 蒸发、分液、蒸馏、过滤 |
5.在室温下,100mL0.1mol/L的醋酸溶液中,欲使其溶液的pH减小,同时又要使醋酸的电离程度减少,可采取( )
| A. | 加入少量CH3COONa固体 | B. | 通入少量HCl气体 | ||
| C. | 升高温度 | D. | 加入少量NaOH固体 |
2.短周期主族元素A、B、C、D的原子序数依次增大.已知A、C的原子序数之差为8,A、B、C三种元素原子的最外层电子数之和为15,B元素原子的最外层电子数等于A元素原子的最外层电子数的一半,下列叙述正确的是( )
| A. | A与C形成的化合物溶于水所得溶液显碱性 | |
| B. | B与D形成的化合物溶于水所得溶液显酸性 | |
| C. | 氢化物的稳定性:C>D | |
| D. | 简单离子的半径:B>C>D>A |
3.在Ag+催化作用下,Cr3+被S2O82-氧化为Cr2O72-的机理为:S2O82-+2Ag+=2SO42-+2Ag2+ 慢2Cr3++6Ag2++7H2O=6Ag++14H++Cr2O72-快下列有关说法正确的是( )
| A. | 反应速率与Ag+浓度有关 | B. | Ag2+也是该反应的催化剂 | ||
| C. | Ag+能降低该反应的活化能和焓变 | D. | v(Cr3+)=v(S2O82-) |