题目内容
(7分)常温下,将0.01 mol CH3COONa和0.002 mol HCl溶于水,形成1 L的混合溶液。
(1)该溶液中存在着三个平衡体系,用电离方程式或离子方程式表示
, , 。
(2)该溶液中,浓度为0.01 mol/L的粒子是 ,浓度为0.002 mol/L的粒子是 。
(3) 和 两种粒子物质的量之和等于0.01 mol。
(1)H2O H++OH-;CH3COOH
H++OH-;CH3COOH CH3COO-+H+;CH3COO-+H2O
CH3COO-+H+;CH3COO-+H2O CH3COOH+OH-;(2)Na+;Cl-;
CH3COOH+OH-;(2)Na+;Cl-;
(3)CH3COOH和CH3COO-
【解析】
试题分析:(1)该溶液中存在水的电离平衡、醋酸的电离平衡、醋酸根离子的水解平衡,分别为H2O H++OH-;CH3COOH
H++OH-;CH3COOH CH3COO-+H+;CH3COO-+H2O
CH3COO-+H+;CH3COO-+H2O CH3COOH+OH-;
CH3COOH+OH-;
(2)由0.01mol CH3COONa,则浓度为0.01molL-1的是Na+,由0.002mol HCl,则浓度为0.002molL-1的是Cl-,答案为Na+;Cl-;
(3)由0.01mol CH3COONa,则CH3COOH、CH3COO-微粒之和为0.01mol,答案为CH3COOH和CH3COO-.
考点:考查溶液中的各种平衡,物质的量浓度的计算等知识。

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案(18分)
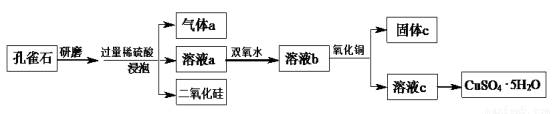
Ⅰ已知:Na2S2O3 + H2SO4 = Na2SO4 + SO2↑ + S↓ + H2O某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
实验序号 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
(1)该实验①、②可探究 对反应速率的影响,因此V1= ,V2= ;V3= ;
(2)实验①、③可探究 对反应速率的影响,因此V4= ,V5= ;
(3)下列有关该的相关叙述正确的是
A.实验前,应先在一张白纸上用黑墨水笔在白纸上画粗浅一致的“+”字,衬在锥形瓶底部,实验中记录反应开始到产生的浑浊将锥形瓶底部的“+”字刚好完全遮盖所需的时间
B.该实验所需的计量仪器有量筒、温度计
C.实验时,应先将量取的Na2S2O3 和H2SO4溶液混合,然后置于相应温度的热水浴中反应,记录每组反应所需时间
D.每组实验至少需要两支量筒
(4)实验过程中为什么不用测量一定时间内放出SO2气体的量来表示该反应的化学反应速率的大小? 。
Ⅱ利用反应:I2+2Na2S2O3=Na2S4O6+2NaI可以定量测定市售硫代硫酸钠(Mr=158)的纯度,现在称取Wg硫代硫酸钠固体样品,配成250mL的溶液,取25.00mL置于锥形瓶中,加入指示剂,用含有I2为amol/L的碘水滴定,消耗碘水bmL,则:
(1)验过程中滴定管应该选择的是 (酸式或碱式)滴定管,滴定前可以选择 做指示剂,滴定终点的现象为
(2)对于该滴定实验的有关操作或误差分析正确的是 。
A.滴定前,应对滴定管、锥形瓶进行润洗操作
B.滴定过程中,标准液滴到锥形瓶外,会使所测结果偏大
C.滴定管在滴定开始时尖嘴有气泡,滴定完成后气泡消失,则所测得的纯度将会偏小
D.滴定前仰视读数而滴定结束时俯视读数,则所测得的纯度将会偏小
(3)样品中硫代硫酸钠纯度的表达式为 。
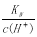 =0.1 mol·L-1的溶液:Na+、AlO2-、CO32-、NO3-
=0.1 mol·L-1的溶液:Na+、AlO2-、CO32-、NO3-