题目内容
14.为提纯如表物质(括号内物质为杂质),所选用的除杂试剂和分离方法正确的是( )| 被提纯的物质 | 除杂试剂 | 分离方法 | |
| A | 乙酸乙酯(乙醇) | 乙酸 | 加热回流 |
| B | 乙烷(乙烯) | 酸性KMnO4 | 洗气 |
| C | 乙醇(乙酸) | 新制氧化钙 | 蒸馏 |
| D | 苯(溴) | 碘化钾溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.乙酸与乙醇的反应为可逆反应;
B.乙烯被高锰酸钾氧化生成二氧化碳;
C.乙酸与CaO反应后,增大与乙醇的沸点差异;
D.溴与KI反应生成的碘易溶于苯.
解答 解:A.乙酸与乙醇的反应为可逆反应,除杂不彻底,应选饱和碳酸钠溶液、分液法分离,故A错误;
B.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,应选溴水、洗气,故B错误;
C.乙酸与CaO反应后,增大与乙醇的沸点差异,然后蒸馏可分离,故C正确;
D.溴与KI反应生成的碘易溶于苯,引入新杂质,应选NaOH溶液、分液,故D错误;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握有机物的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意除杂的原则,题目难度不大.

练习册系列答案
相关题目
4.如图装置在化学工业中有广泛应用.X、Y是两块石墨,通过导线与直流电源相连.下列说法错误的( )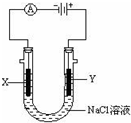

| A. | 该装置发生了化学变化 | B. | 该装置可获得氯气 | ||
| C. | 该装置可获得金属钠 | D. | 溶液中的Na+向X极移动 |
5.向一固定体积的密闭容器中通入a mol N2O4气体,在密闭容器内发生反应:N2O4(g)?2NO2(g),达到平衡时再通入a mol N2O4气体,再次达到平衡时,与第一次达平衡时相比,N2O4的转化率( )
| A. | 不变 | B. | 增大 | C. | 减小 | D. | 无法判断 |
9.下列说法正确的是( )
| A. | 纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 | |
| B. | 油脂都不能使溴的四氯化碳溶液褪色 | |
| C. | 石油分馏、煤的干馏均为物理变化 | |
| D. | 淀粉、蛋白质和天然橡胶均是天然高分子化合物 |
6.资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学设计了如下实验方案并验证产物、探究反应原理.
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能为Mg(OH)2;
猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3•yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
(3)为进一步确定实验1的产物,设计定量实验方案,如图所示: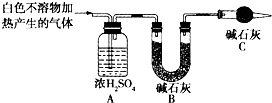
称取实验1中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部通入装置A和B中.实验后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式:Mg(OH)2(CO3)2或2MgCO3•Mg(OH)2 ;
(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡和白色不溶物的原因:NaHCO3溶液中存在平衡,HCO3-?H++CO32-、H2O?H++OH-;Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)2•2MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行.
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能为Mg(OH)2;
猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3•yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | 气体成分为 ①氢气 |
| 实验Ⅲ | 取实验Ⅰ中的白色不溶物,洗涤,加入足量 ②稀盐酸 | ③产生气泡沉淀全部溶解 | 白色不溶物可能含有猜测2中不溶物 |
| 实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 产生白色沉淀 | 溶液中存在 ④CO32- |

称取实验1中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部通入装置A和B中.实验后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式:Mg(OH)2(CO3)2或2MgCO3•Mg(OH)2 ;
(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡和白色不溶物的原因:NaHCO3溶液中存在平衡,HCO3-?H++CO32-、H2O?H++OH-;Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)2•2MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行.
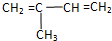 ⑤
⑤ ⑥CH3CH(C2H5)CH2CH(C2H5)CH3⑦C5H10⑧ClCH═CHCl
⑥CH3CH(C2H5)CH2CH(C2H5)CH3⑦C5H10⑧ClCH═CHCl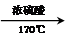 CH2═CH2↑+H2O.
CH2═CH2↑+H2O. .
. CO(g)+H2(g) ΔH=+131.3KJ/mol,反应的平衡常数表达式为K= 。
CO(g)+H2(g) ΔH=+131.3KJ/mol,反应的平衡常数表达式为K= 。