题目内容
将钠、镁、铝各0.3 mol,分别放入100 mL 1 mol·L—1的硫酸中,同温同压下产生的气体的体积比是
A.1∶2∶3 B.6∶3∶2 C.3∶2∶2 D.3∶1∶1
C
【解析】
试题分析:Mg+2H+=Mg2++H2↑、2Al+6H+=2Al3++3H2↑、2Na+2H+=2Na++H2↑、2Na+2H2O=2NaOH+H2↑由以上反应方程式可知,镁、铝在与酸的反应过程中均过量,产生的氢气均为0.1mol,但钠除了可与硫酸反应外,还可与溶剂水反应,最终全部转换为氢气,可得氢气为0.15mol,故同温同压下产生的气体的体积比为3∶2∶2(等于物质的量之比)。
考点:钠镁铝的性质

练习册系列答案
相关题目
下列实验操作完全正确的是
编号 | 实验 | 操作 |
A. | 钠与水反应 | 用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
B. | 配制一定浓度的氯化钾溶液1000mL | 准确称取氯化钾固体,放入到1000ml的容量瓶中,加水溶解,振荡摇匀,定容 |
C. | 证明某溶液中含Fe2+ | 取少量该溶液先加入氯水,再滴加KSCN溶液 |
D. | 取出分液漏斗中的上层液体 | 下层液体从分液漏斗下端管口放出,及时关闭活塞,换一个接收容器,上层液体从分液漏斗上口倒出 |
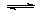 2SO3(g) ΔH= -196.6kJ·mol-1
2SO3(g) ΔH= -196.6kJ·mol-1