题目内容
11.下列各组物质:①O2和O3;
②乙烷和丁烷;
③12C和14C;
④CH3COOH和HCOOCH3
⑤
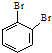 和
和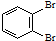
⑥
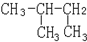 和
和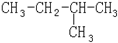
(用上述物质序号填空)
互为同系物的是②,互为同分异构体的是④,互为同位素的是③,互为同素异形体的是①.
分析 具有相同质子数,不同中子数的同一元素的不同核素互为同位素;
具有相同分子式而结构不同的化合物互为同分异构体;
结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物;
相同元素组成,不同形态的单质互为同素异形体.
解答 解:①O2和O3都是由氧元素形成的不同单质,互为同素异形体;
②乙烷和丁烷都是烷烃,结构相似,分子组成相差2个“CH2”原子团,互为同系物;
③12C和14C是碳元素的不同种原子,互为同位素;
④CH3COOH和HCOOCH3的分子式相同而结构不同,故互为同分异构体.
⑤ 和
和 的分子式相同,结构相同,是同一种化合物;
的分子式相同,结构相同,是同一种化合物;
⑥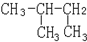 和
和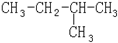 的分子式相同,结构相同,是同一种化合物;
的分子式相同,结构相同,是同一种化合物;
故答案为:②;④;③;①.
点评 本题考查同分异构体、同位素、同素异形体、同一物质等,难度不大,注意把握概念的内涵与外延.

练习册系列答案
相关题目
9.下列叙述中,正确的是( )
| A. | 将0.l mol•L-1醋酸溶液加水稀释,溶液中所有离子的浓度都减小 | |
| B. | 0.1 mol/L的一元弱酸HA加水稀释过程中,$\frac{c({A}^{-})}{c(HA)•c(O{H}^{-})}$ 不变 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 中和10 mL 0.1mol•L-1醋酸与中和100 mL 0.01mol•L-1的醋酸所需同种碱液的量不同 |
19.下列关于化石燃料的加工的说法正确的是( )
| A. | 石油裂化主要得到乙烯 | |
| B. | 石油分馏是化学变化,可得到汽油、煤油 | |
| C. | 煤的干馏是化学变化,可以得到出炉煤气、煤焦油和焦炭 | |
| D. | 煤的气化是物理变化,是高效、清洁地利用煤的途径 |
16.已知氢气和气态碘在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-a kJ•moL-1
已知: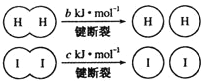
(a、b、c均大于零)下列说法中正确的是( )
已知:

(a、b、c均大于零)下列说法中正确的是( )
| A. | 向密闭容器中加入1 mol H2(g)和2mol I2(g),充分反应后放出的热量有可能等于a kJ | |
| B. | 反应物的总能量低于生成物的总能量 | |
| C. | 断开2 mol H-I键所需能量约为(c+b+a)kJ | |
| D. | 断开1 mol I-I键的同时形成2mol H-I键,说明反应已达到平衡状态 |
1. A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A与D同主族;C与E同主族;B、C同周期;B原子最外层电子数比其次外层电子数多2;A是周期表中半径最小的元素,C的最外层电子数是内层电子的3倍;F元素是同周期元素中原子半径最小的主族元素.A、B、C、D、E形成的化合物甲、乙、丙、丁的组成如表所示:
A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A与D同主族;C与E同主族;B、C同周期;B原子最外层电子数比其次外层电子数多2;A是周期表中半径最小的元素,C的最外层电子数是内层电子的3倍;F元素是同周期元素中原子半径最小的主族元素.A、B、C、D、E形成的化合物甲、乙、丙、丁的组成如表所示:
回答下列问题:
(1)指出元素F在周期表中的位置第三周期第ⅦA族.
(2)化合物乙的电子式为 ,用电子式表示形成化合物丁的过程
,用电子式表示形成化合物丁的过程
(3)写出丙与甲反应的离子方程式:2Na2O2+2H2O=4Na++4OH -+O2↑.
(4)固体氧化物燃料电池是以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许O2-在其间通过,该电池的工作原理如图所示,其中多孔Pt电极a、b分别是气体C2、A2的载体.该电池的负极为b(填a或b);O2-流向负极(填“正”或“负”);该电池的正极反应式为O2+4 e-=2O2-.
 A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A与D同主族;C与E同主族;B、C同周期;B原子最外层电子数比其次外层电子数多2;A是周期表中半径最小的元素,C的最外层电子数是内层电子的3倍;F元素是同周期元素中原子半径最小的主族元素.A、B、C、D、E形成的化合物甲、乙、丙、丁的组成如表所示:
A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A与D同主族;C与E同主族;B、C同周期;B原子最外层电子数比其次外层电子数多2;A是周期表中半径最小的元素,C的最外层电子数是内层电子的3倍;F元素是同周期元素中原子半径最小的主族元素.A、B、C、D、E形成的化合物甲、乙、丙、丁的组成如表所示:| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 化学式 | A2C | A2C2 | D2C2 | D2E |
(1)指出元素F在周期表中的位置第三周期第ⅦA族.
(2)化合物乙的电子式为
 ,用电子式表示形成化合物丁的过程
,用电子式表示形成化合物丁的过程
(3)写出丙与甲反应的离子方程式:2Na2O2+2H2O=4Na++4OH -+O2↑.
(4)固体氧化物燃料电池是以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许O2-在其间通过,该电池的工作原理如图所示,其中多孔Pt电极a、b分别是气体C2、A2的载体.该电池的负极为b(填a或b);O2-流向负极(填“正”或“负”);该电池的正极反应式为O2+4 e-=2O2-.
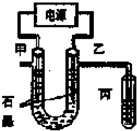 CuCl2溶液中的铜主要以Cu (H2O)42+、CuCl42-形式存在,它们间有如下转化关系:Cu(H2O)42+(蓝色)+4Cl-?CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电.下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝.回答下列问题:
CuCl2溶液中的铜主要以Cu (H2O)42+、CuCl42-形式存在,它们间有如下转化关系:Cu(H2O)42+(蓝色)+4Cl-?CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电.下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝.回答下列问题: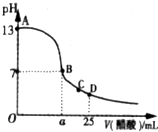 在25mL的氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,滴定曲线如图所示.
在25mL的氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,滴定曲线如图所示.

 .
.